题目内容
19.室温下pH值相同的下列溶液中,浓度最大的是( )| A. | Na2CO3 | B. | NaHCO3 | C. | NaOH | D. | CH3COONa |
分析 盐的水解规律:有弱才水解,无弱不水解,谁强显谁性,越弱越水解,酸越弱对应盐水解程度越大,pH值相同的下列溶液中水解程度越大,其溶质浓度越小.
解答 解:氢氧化钠为强碱,溶液PH相同时,浓度最小,酸性强弱为CH3COOH>H2CO3>HCO3-,其盐水解的水解程度CH3COONa<NaHCO3<Na2CO3,室温下pH值相同的溶液中,醋酸钠浓度最大,故选D.
点评 本题考查盐的水解.相同温度下,物质的量浓度相同的盐溶液,盐的组成中酸根离子对应的酸越弱,盐溶液中酸根离子水解程度越大,溶液pH越大,PH相同水解程度越大的溶质浓度越小,题目难度中等.

练习册系列答案
相关题目
17.在常温下,分别利用下列反应产生氢气,其反应方程式分别为:
①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O
如果上述两个反应所产生的氯气质量相等,被氧化的还原剂的物质的量之比为( )
①2KMnO4+16HCl(浓)→2KCl+2MnCl2+5Cl2↑+8H2O
②KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O
如果上述两个反应所产生的氯气质量相等,被氧化的还原剂的物质的量之比为( )
| A. | 8:5 | B. | 6:5 | C. | 2:1 | D. | 1:1 |
7.将下列离子:Al3+、Na+、K+、NO3-、OH-、S2-、MnO4-、Fe3+、NH4+、H+、AlO2-、CO32-按可能大量共存的情况,把它们全部分成A、B两组,而且每组中都含有不少于两种阳离子和两种阴离子.下列离子不会同在一组的是( )
| A. | Na+、NO3- | B. | S2-、AlO2- | C. | Al3+、Fe3+ | D. | MnO4-、NH4+ |
14.在恒温恒容密闭容器中,不能说明反应2NO2(g)?2NO(g)+O2(g)达到平衡状态的是( )
| A. | NO2、NO、O2的物质的量之比是2:1:1 | |
| B. | 单位时间内生成1mol O2的同时生成2mol NO2 | |
| C. | 混合气体的颜色不再改变的状态 | |
| D. | 混合气体的平均相对分子质量不再改变的状态 |
4.下列有关物质的性质和用途的说法正确的是( )
| A. | 一定条件下,用秸秆可制得葡萄糖和酒精 | |
| B. | 铁制品表面涂“银粉”(铝粉)防生锈,是由于铝的化学性质比铁的稳定 | |
| C. | 氧气被用作火箭的燃料,利用了氧气的可燃性 | |
| D. | 稀有气体充入霓虹灯,利用了稀有气体通电时发出不同颜色的光的化学性质 |
11.科学家成功开发出便携式固体氧化物燃料电池,它以丙烷气体为燃料,空气为氧化剂,电解质是固态氧化物,在熔融状态下能传导O2-; 该电池的总反应是C3H8+5O2═3CO2+4H2O,负极反应为C3H8-20e-+10O2-═3CO2+4H2O.下列关于该燃料电池的说法中正确的是( )
| A. | 在熔融电解质中,O2-由负极移向正极 | |
| B. | 电池的正极通入丙烷 | |
| C. | 电路中每通过5 mol 电子,约有5.6 L标准状况下的丙烷被完全氧化 | |
| D. | 在电池正极的电极反应为O2-4e-═2O2- |
9.已知苯乙烯的结构为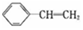 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )
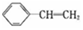 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )| A. | 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物有6种 | |
| B. | 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同 | |
| C. | 苯乙烯分子的所有原子不可能在同一平面上 | |
| D. | 除去 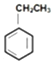 中的苯乙烯可以通入等量氢气反应 中的苯乙烯可以通入等量氢气反应 |
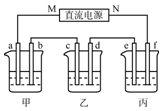 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5%的NaOH溶液、足量的CuSO4溶液和10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5%的NaOH溶液、足量的CuSO4溶液和10.00%的K2SO4溶液,电极均为石墨电极.