题目内容
1.下列操作能达到实验目的且符合实验室安全措施的是( )| A. | 稀释浓硫酸,应将水慢慢注入盛有浓硫酸的烧杯中并搅拌 | |
| B. | 酒精灯洒出的酒精万一在桌上着火,应立即用湿抹布扑盖 | |
| C. | 碱溶液沾到皮肤上,应尽快用抹布擦拭干净,再涂上稀盐酸 | |
| D. | 氢气还原氧化铜实验结束时,为节约氢气,应先停止氢气再停止加热 |
分析 A.浓硫酸密度大于水,应该将浓硫酸倒入水中,顺序不能颠倒;
B.酒精密度小于水,不能用水灭火,可以用湿抹布盖灭;
C.稀盐酸检验腐蚀性,不能用稀盐酸中和皮肤上的碱液,可以使用硼酸;
D.为了防止生成的铜被氧化,应该先停止加热再停止通入氢气.
解答 解:A.稀释浓硫酸时,由于水的密度小于浓硫酸,且浓硫酸稀释放出大量热,所以应该将浓硫酸慢慢倒入水中,否则容易造成酸液飞溅,发生危险,故A错误;
B.酒精着火,由于水的密度大于酒精,所以不能使用水灭火,可以使用湿抹布盖灭,故B正确;
C.稀盐酸检验腐蚀性,不能涂上稀盐酸,可以涂上弱酸硼酸进行中和碱液,故C错误;
D.为了防止生成的铜被氧化,应该先停止加热,待冷却后再停止通入氢气,故D错误;
故选B.
点评 本题考查化学实验方案的评价,题目难度不大,旨在考查学生的基础知识的掌握,化学实验是化学的基础,要了解常见的实验操作,能对错误操作的后果做出判断,养成良好的实验习惯.

练习册系列答案
相关题目
18.A、B、C、D、E为原子序数依次增大的短周期主族元素,A与C、B与D分别同主族,且A、C元素的质子数之和是B、D元素质子数之和的一半.下列判断正确的是( )
| A. | 原子半径大小顺序:D>C>B>A | |
| B. | 由B和C元素组成的化合物,可以既含有离子键,又含有共价键 | |
| C. | 元素B、D、E分别与A形成的化合物中,熔沸点最低的是B与A形成的化合物 | |
| D. | 元素D与C形成的化合物在空气中长期放置不易变质 |
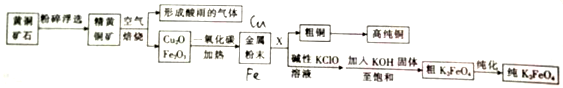
9.下列装置图及有关说法正确的是( )
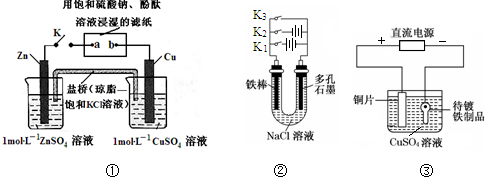

| A. | 装置①中K键闭合时,片刻后可观察到滤纸a点变红色 | |
| B. | 装置①中K键闭合时,片刻后CuSO4溶液中c(Cl-)增大 | |
| C. | 装置②中铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>只闭合K2>都断开 | |
| D. | 装置③中当铁制品上析出1.6 g铜时,电源负极输出的电子数为0.025 NA |
16.玻璃的主要成分是二氧化硅,能在玻璃上进行雕刻的物质是( )
| A. | 纯碱 | B. | 盐酸 | C. | 氢氟酸 | D. | 硫酸 |
6.在电解冶炼铝的电解槽中存在电解质W2[X2Y2Z4].已知其涉及的四种元素的简单离子的电子层结构均相同,Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半.下列说法正确的是( )
| A. | 原子序数:W>X>Y>Z | B. | 原子半径:W>X>Y>Z | ||
| C. | W的最高价氢氧化物的碱性比X弱 | D. | Y的最简单氢化物的稳定性比Z的强 |
13.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在pH=1的溶液中:K+、Na+、SO42-、HCO3- | |
| B. | 在0.1 mol•L-1 Na2CO3溶液中:Al3+、K+、NO3-、SO42- | |
| C. | 在0.1 mol•L-1 FeCl3溶液中:K+、NH4+、I-、SCN- | |
| D. | 在$\frac{c({H}^{+})}{c(OH)}$=10-12的溶液中:K+、Na+、ClO-、NO3- |
11.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 物质 | 试剂 | 分离方法 | |
| A | 硝酸钾(氯化钠) | 蒸馏水 | 降温结晶 |
| B | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 氢氧化钠(氢氧化钡) | 稀硫酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
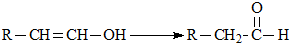 化学式为C9H10O2的有机物A有如下的转化关系
化学式为C9H10O2的有机物A有如下的转化关系
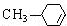 ,H:CH3COOCH=CH2
,H:CH3COOCH=CH2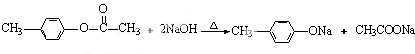
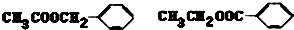 .
.