题目内容
6.在电解冶炼铝的电解槽中存在电解质W2[X2Y2Z4].已知其涉及的四种元素的简单离子的电子层结构均相同,Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半.下列说法正确的是( )| A. | 原子序数:W>X>Y>Z | B. | 原子半径:W>X>Y>Z | ||
| C. | W的最高价氢氧化物的碱性比X弱 | D. | Y的最简单氢化物的稳定性比Z的强 |
分析 在电治铝的电解槽中存在电解质W2[X2Y2Z4],四种元素的简单离子的电子层结构均相同,Y原子最外层电子数为次外层的3倍,原子只能有2个电子层,最外层电子数为6,故Y为O元素;X原子最外层电子数为Y原子最外层电子数的一半,其最外层电子数为3,则X为Al;该化合物中W应该带正电荷,含有两个铝离子、两个O离子,Z应该带负电荷,根据化合物代数和为0知,W应该带一个单位正电荷,Z带一个单位负电荷,且这四种简单离子电子层结构相同,所以W为Na、Z为F元素,则该电解质为Na2[Al2O2F4].
A.通过以上分析判断原子序数;
B.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强;
D.元素的非金属性越强,其气态氢化物的稳定性越强.
解答 解:在电治铝的电解槽中存在电解质W2[X2Y2Z4],四种元素的简单离子的电子层结构均相同,Y原子最外层电子数为次外层的3倍,原子只能有2个电子层,最外层电子数为6,故Y为O元素;X原子最外层电子数为Y原子最外层电子数的一半,其最外层电子数为3,则X为Al;该化合物中W应该带正电荷,含有两个铝离子、两个O离子,Z应该带负电荷,根据化合物代数和为0知,W应该带一个单位正电荷,Z带一个单位负电荷,且这四种简单离子电子层结构相同,所以W为Na、Z为F元素,则该电解质为Na2[Al2O2F4].
A.通过以上分析知,原子序数X>W>Z>Y,故A错误;
B.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径:W(Na)>X(Al)>Y(O)>Z(F),故B正确;
C.元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性W>X,所以W的最高价氧化物的水化物碱性比X的强,故C错误;
D.元素的非金属性越强,其气态氢化物的稳定性越强,非金属性Z>Y,所以Y的简单氢化物的稳定性比Z的弱,故D错误;
故选B.
点评 本题考查原子结构、元素周期律,侧重考查分析推断综合应用能力,正确推断元素是解本题关键,熟练掌握元素周期律知识,题目难度中等.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案C6H12O6(葡萄糖)+Br2+H2O-→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3-→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

(1)第①步中溴水氧化葡萄糖时,下列装置中最适合的是B.
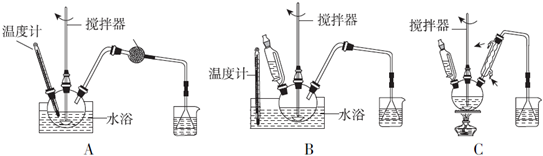
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是C.
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率;本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应得到葡萄糖酸钙.
(3)第③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品.
(4)第④步加入乙醇的作用是可降低葡萄糖酸钙在溶剂中的溶解度,有利于葡萄糖酸钙的析出.
(5)第⑥步中,下列洗涤剂最合适的是D.
A.冷水 B.热水 C.乙醇 D.乙醇水混合溶液.
| A. | B与A只能组成BA3化合物 | |
| B. | 第三周期中,D原子的原子半径最大 | |
| C. | A、B、C三元素不可能形成离子化合物 | |
| D. | E的氧化物对应水化物一定有强的氧化性 |
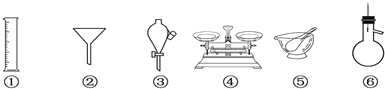
| A. | ①③⑥ | B. | ②④⑥ | C. | ②③⑥ | D. | ②③⑤ |
| A. | 稀释浓硫酸,应将水慢慢注入盛有浓硫酸的烧杯中并搅拌 | |
| B. | 酒精灯洒出的酒精万一在桌上着火,应立即用湿抹布扑盖 | |
| C. | 碱溶液沾到皮肤上,应尽快用抹布擦拭干净,再涂上稀盐酸 | |
| D. | 氢气还原氧化铜实验结束时,为节约氢气,应先停止氢气再停止加热 |
| A. | 原子序数:A>C>B>D | B. | 原子半径:B>D>C>A | ||
| C. | 原子序数:C>B>D>A | D. | 简单离子半径:D>B>C>A |
| A. | 100 mL 0.8 mol•L-1MgCl2溶液 | B. | 200 mL 0.4 mol•L-1AlCl3溶液 | ||
| C. | 50 mL 1.6 mol•L-1NaCl溶液 | D. | 25 mL 0.8 mol•L-1HCl溶液 |
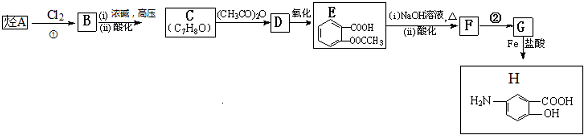
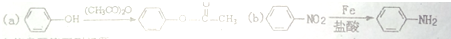
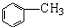 ,F含有的官能团是羧基和酚羟基(填名称).
,F含有的官能团是羧基和酚羟基(填名称).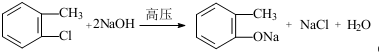 .
.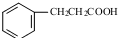 .
.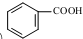 发生取代时,在羧基间位取代;②
发生取代时,在羧基间位取代;②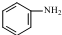 易发生氧化反应.以A为原料合成化合物
易发生氧化反应.以A为原料合成化合物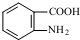 的设计合成路线为(其他试剂任选):
的设计合成路线为(其他试剂任选):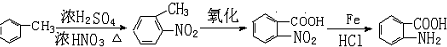 .
.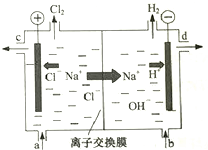 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空: