题目内容
16.玻璃的主要成分是二氧化硅,能在玻璃上进行雕刻的物质是( )| A. | 纯碱 | B. | 盐酸 | C. | 氢氟酸 | D. | 硫酸 |
分析 二氧化硅性质较为稳定,与硝酸、硫酸、盐酸以及强氧化性物质不反应,在一定条件下可与碱、碱性氧化物、盐以及HF酸反应.
解答 解:A.纯碱与二氧化硅在高温下反应,不能用于在玻璃上进行刻蚀,故A错误;
B.盐酸和二氧化硅不反应,不能用于在玻璃上进行刻蚀,故B错误;
C.氢氟酸与二氧化硅易反应,生产四氟化硅气体,能在玻璃上进行刻蚀,故C正确;
D.硫酸和二氧化硅不反应,不能用于在玻璃上进行刻蚀,故D错误.
故选C.
点评 本题考查二氧化硅的性质,题目难度不大,以识记为主,旨在考查学生对教材中基础知识的积累.

练习册系列答案
相关题目
11.下列有关化学反应表达正确的是( )
| A. | 实验室用液溴和苯在催化剂作用下制溴苯: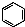 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$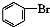 +HBr +HBr | |
| B. | 蛋壳溶于食醋:CaCO3+CH3COOH=CH3COOCa+H2O+CO2↑ | |
| C. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O | |
| D. | 向氯乙烷水溶液中加入氢氧化钠溶液共热:CH3CH2Cl+NaOH$\stackrel{△}{→}$CH2=CH2+NaCl+H2O |
1.下列操作能达到实验目的且符合实验室安全措施的是( )
| A. | 稀释浓硫酸,应将水慢慢注入盛有浓硫酸的烧杯中并搅拌 | |
| B. | 酒精灯洒出的酒精万一在桌上着火,应立即用湿抹布扑盖 | |
| C. | 碱溶液沾到皮肤上,应尽快用抹布擦拭干净,再涂上稀盐酸 | |
| D. | 氢气还原氧化铜实验结束时,为节约氢气,应先停止氢气再停止加热 |
8.在固态金属氧化物电解池中,高温共电解H20-CO2湿合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
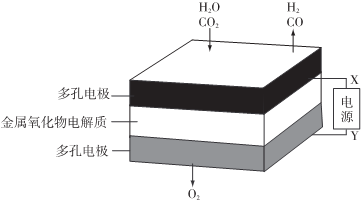

| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2- | |
| C. | 总反应可表示为:H2O+CO2═H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是1:2 |
5.下列溶液中,C(OH-)最小的是( )
| A. | 向0.1mol•L-1的氨水中加入同体积的水 | |
| B. | 向0.1mol•L-1的KOH溶液中加入同体积的水 | |
| C. | 向0.2mol•L-1的氨水中加入同体积的0.1mol•L-1盐酸 | |
| D. | 向0.2mol•L-1的KOH溶液中加入同体积的0.1mol•L-1盐酸 |
6.下列有关物质性质或应用的说法正确的是( )
| A. | 医疗上,常用碳酸钠治疗胃酸过多 | |
| B. | 在海轮外壳上安装锌块以减缓船体腐蚀 | |
| C. | 液氨汽化放出大量的热,可用作制冷剂 | |
| D. | 明矾具有强氧化性,常用于自来水的杀菌消毒 |
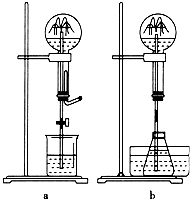 喷泉是一种常见的自然现象,其产生原因通常是装置内外存在压强差.
喷泉是一种常见的自然现象,其产生原因通常是装置内外存在压强差.