题目内容
20.利尿酸在奥运会上被禁用,其结构简式如图所示.下列叙述正确的是( )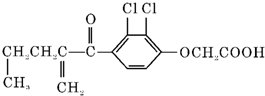
| A. | 利尿酸的衍生物利尿酸甲酯的分子式是C14H14O4Cl2 | |
| B. | 利尿酸不能发生酯化反应 | |
| C. | 1 mol利尿酸能与7 mol H2发生加成反应 | |
| D. | 利尿酸不能与FeCl3溶液发生显色反应 |
分析 由结构可知分子式,分子中含碳碳双键、-Cl、-COOH及羰基、醚键等,结合烯烃、卤代烃及羧酸的性质来解答.
解答 解:A.由结构可知利尿酸的分子式为C14H14O4Cl2,利尿酸甲酯的分子式是C15H16O4Cl2,故A错误;
B.含-COOH,可发生酯化反应,故B错误;
C.苯环、碳碳双键、羰基与氢气发生加成反应,则1 mol利尿酸能与5 mol H2发生加成反应,故C错误;
D.不含酚-OH,则利尿酸不能与FeCl3溶液发生显色反应,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、羧酸的性质及应用,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
10.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | Na、Mg、Al的第一电离能逐渐增大 | B. | 热稳定性:HF>H2O>NH3 | ||
| C. | S2-、Cl-、K+的半径逐渐增大 | D. | O、F、Ne的电负性逐渐增大 |
11.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18g D2O所含电子数目为10NA | |
| B. | 实验室用含2molHCl的浓盐酸在加热下与足量的MnO2反应,转移的电子数为NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为4NA | |
| D. | 标准状况下,22.4 L氦气与18g水所含分子数均为NA |
5.用NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 14 g乙烯和丙烯的混合物中总原子数为3NA个 | |
| B. | 106gNa2CO3固体中含有NA个CO32- | |
| C. | 200mL0.5 mol•L-1的Na2CO3溶液中阴离子数目小于0.1 NA | |
| D. | 常温下,1 mol Cu和足量浓硝酸反应可收集NO2的分子数小于2NA |
9.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,8.8g CO2和N2O混合物中所含有的原子数为0.6 NA | |
| B. | 二氧化锰和浓盐酸反应产生4.48L气体时,转移的电子数为0.4NA | |
| C. | 标准状况下,3.36L水中含有电子数为1.5NA | |
| D. | 在0.2mol/L的硫酸铁溶液中含有的三价铁离子数为0.6 NA |
10.化学在生产和日常生活中有着重要的应用.下列说法中不正确的是( )
| A. | 铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀 | |
| B. | 铝热反应不仅被用于焊接钢轨,而且还常被用于冶炼熔点较高的金属 | |
| C. | 电解AlCl3饱和溶液,可制得金属铝 | |
| D. | Al2O3、MgO的熔点很高,可用于制作耐高温材料 |