题目内容
8.在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.(1)某厂废水中含KCN,其浓度为650mg/L.现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O,被氧化的元素是C.
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气.请配平下列化学方程式,并标出电子转移方向和数目:
2KOCN+4KOH+3Cl2→2CO2+1N2+6KCl+2H2O
(3)若处理上述废水100L,使KCN完全转化为无毒物质,至少需液氯175.5 g.
分析 (1)化合价升高的元素被氧化;
(2)反应中KOCN→N2,N元素化合价由-3价升高为0价,共升高6价,Cl2→KCl,Cl元素化合价由0价降低为-1价,共降低2价,化合价升降最小公倍数为6,故N2系数为1,Cl2系数为3,结合原子守恒配平其它物质的系数;
(3)计算废水中KCN的质量,再根据n=$\frac{m}{M}$计算KCN的物质的量,使KCN完全转化为无毒物质,生成CO、
N2,整个过程中C元素化合价由+2价升高为+4价,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,根据电子转移守恒计算n(Cl2),再根据m=nM计算需要氯气的质量
解答 解:(1)反应中C元素化合价由KCN中+2价升高为KOCN中+4价,C元素被氧化,
故答案为:C;
(2)反应中KOCN→N2,N元素化合价由-3价升高为0价,共升高6价,Cl2→KCl,Cl元素化合价由0价降低为-1价,共降低2价,化合价升降最小公倍数为6,故N2系数为1,Cl2系数为3,结合原子守恒配平其它物质的系数,平衡后方程式为:2KOCN+4KOH+3Cl2═2CO2+N2+6KCl+2H2O,电子转移的方向和数目为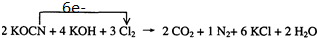
故答案为:2、4、3、2、1、6、2;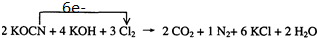 ;
;
(3)废水中KCN的质量为650mg/L×100L=13000mg=65g,物质的量为$\frac{65g}{65g/mol}$=1mol,使KCN完全转化为无毒物质,应生成CO、N2,整个过程中C元素化合价由+2价升高为+4价,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,电子转移守恒可知2×n(Cl2)=1mol×(4-2)+1mol×[0-(-3)],解得n(Cl2)=2.5mol,故需要氯气的质量为2.5mol×71g/mol=175.5g,
故答案为:175.5.
点评 本题综合考查学生的分析能力和计算能力,为高频考点,注意把握元素化合价的判断,为解答该题的关键,结合电子得失守恒解答该题,难度不大

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 此有机物一定是烃CH4 | D. | 分子中可能含有氧原子 |
| A. | 50g质量分数为17%的H2O2水溶液中含氧原子数目为0.5NA | |
| B. |  12g石墨烯(如图)中含有C-C键的数目为1.5NA 12g石墨烯(如图)中含有C-C键的数目为1.5NA | |
| C. | 常温下,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | 一定量的Na2O2与H2O反应产生1.12L O2,则反应中转移的电子数为0.1NA |
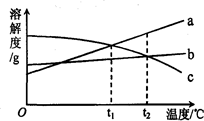 a、b、c三种物质的溶解度曲线如图所示.取等质量t2℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t2℃.下列说法不正确的是
a、b、c三种物质的溶解度曲线如图所示.取等质量t2℃的a、b、c三种物质的饱和溶液,分别蒸发等量水后恢复至t2℃.下列说法不正确的是( )
| A. | 原饱和溶液中,溶质的质量分数a>b=c | |
| B. | 恢复至t2℃时,析出溶质的质量a>b=c | |
| C. | 恢复至t2℃时,三种溶液一定都是饱和溶液 | |
| D. | 若继续降温至t1℃,三种溶液一定都是饱和溶液 |
| A. | NaCl溶液(BaCl2),加Na2SO4溶液,过滤 | |
| B. | KNO3溶液(AgNO3),加KCl溶液,过滤 | |
| C. | NaCl溶液(I2),加酒精,分液 | |
| D. | KNO3溶液(I2),加四氯化碳,分液 |
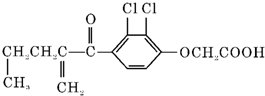
| A. | 利尿酸的衍生物利尿酸甲酯的分子式是C14H14O4Cl2 | |
| B. | 利尿酸不能发生酯化反应 | |
| C. | 1 mol利尿酸能与7 mol H2发生加成反应 | |
| D. | 利尿酸不能与FeCl3溶液发生显色反应 |
| A. | C5H10 | B. | 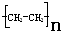 | C. | CH4O | D. | C2H4Cl2 |
| A. | 原电池是将电能转化为化学能的过程 | |
| B. | 煤燃烧是化学能转化为热能的过程 | |
| C. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| D. | 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |