题目内容
4.已知有下列物质:①碳酸氢钠粉末 ②铜丝 ③稀硫酸溶液 ④CO2(1)属于电解质的是:①(填序号,下同);
(2)属于非电解质的是:④;
(3)碳酸氢钠在水中的电离方程式:NaHCO3═Na++HCO3-.
分析 在水溶液中或者熔融状态下能够导电的化合物为电解质;
在水溶液中和熔融状态下都不能够导电的化合物为非电解质;
单质和混合物既不是电解质,也不是非电解质;
碳酸氢钠为强电解质,完全电离.
解答 解:①碳酸氢钠粉末是在水溶液中或者熔融状态下能够导电的化合物为电解质;
②铜丝是单质既不是电解质,也不是非电解质;
③稀硫酸溶液是混合物既不是电解质,也不是非电解质;
④CO2本身不能电离的化合物,属于非电解质;
所以属于电解质的是:①;
属于非电解质的是:④;
碳酸氢钠为强电解质,完全电离,电离方程式:NaHCO3═Na++HCO3-;
故答案为:(1)①;
(2)④;
(3)NaHCO3═Na++HCO3-.
点评 本题考查了电解质、非电解质判断及电离方程式的书写,明确电解质、非电解质概念及电离方式是解题关键,题目难度不大,注意单质和混合物既不是电解质,也不是非电解质.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
1.在一定条件下,PbO2与浓盐酸反应,产物是Cl2和Pb2+,则生成0.1mol Cl2所需PbO2的物质的量为( )
| A. | 0.3mol | B. | 0.15mol | C. | 0.1mol | D. | 0.075mol |
15.下列的分离方法正确的是( )
| A. | 除去 KCl中的K2CO3可先加入过量的BaCl2溶液,待沉淀完全后再过滤、洗涤,取滤液蒸发即得纯净的KCl | |
| B. | 氯化钠的溶解度随着温度下降而减少,用冷却结晶法从热的含有少量氯化钾浓溶液中可得到纯净的氯化钠 | |
| C. | 除去Cu粉中混有的少量Fe粉可加入过量的稀盐酸,待无气泡产生后过滤烘干即可 | |
| D. | 通过点燃可除去二氧化碳中混有的CO气体 |
12.硅及其化合物是重要的无机材料,其中光导纤维的成份是( )
| A. | 硅 | B. | 二氧化硅 | C. | 硅酸钠 | D. | 硅酸 |
19.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,5.6L CO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 2L 0.5 mol•L-1 亚硫酸溶液中含有的H+数为2NA | |
| C. | 分子总数为NA的SO2和CO2混合气体中含有的氧原子数为2NA | |
| D. | 1mol FeI2与足量氯气反应时转移的电子数为2NA |
13.金刚烷的结构如图所示,其二氯代物有(不考虑立体异构)( )
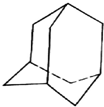

| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
14.化学与日常生活紧密相关,下列说法错误的是( )
| A. | 氮肥NH4NO3在重力撞击下可能发生爆炸 | |
| B. | 在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮 | |
| C. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 | |
| D. | 碳酸氢钠可用来治疗胃酸过多 |
 前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.回答下列问题:
前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.回答下列问题: .
.