题目内容
1.根据化学反应3NO2+H2O→2HNO3+X,推断X的化学式为( )| A. | NO | B. | N2 | C. | N2O3 | D. | N2O5 |
分析 由NO2→HNO3可知,N元素的化合价由+4价升高为+5价,则X中N元素的化合价小于+4,结合电子守恒计算.
解答 解:由NO2→HNO3可知,N元素的化合价由+4价升高为+5价,则X中N元素的化合价小于+4,
设X中N元素的化合价为x,由电子守恒可知,
2×(5-4)=1×(4-x),
解得x=2,
只有NO中N元素的化合价为+2价,
故选A.
点评 本题考查氧化还原反应计算,为高频考点,把握反应中元素的化合价变化及电子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
11.下列各组顺序的排列不正确的是( )
| A. | 原子半径:Na>Mg>Al | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H3PO4 | D. | 熔点:Na>K>Rb |
12.将盛有12mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积和剩余的2mL气体分别是( )
| A. | 1.2 mL,NO | B. | 2.4 mL,O2 | C. | 3.5 mL,O2 | D. | 4 mL,NO |
9.下列萃取和分液结合进行的操作(用CCl4从碘水中萃取碘)中错误的是( )
| A. | 饱和碘水和CCl4加入分液漏斗中后,盖上玻璃塞,用右手压住分液漏斗玻璃塞,左手握住活塞部分,把分液漏斗倒转过来振荡 | |
| B. | 静置前,先使分液漏斗内外空气相通,溶液分层 | |
| C. | 打开分液漏斗的活塞,使下层液体沿烧杯内壁慢慢流出,下层液体放完时立即关闭活塞 | |
| D. | 最后再打开分液漏斗的活塞,放出并保存上层液 |
13.根据元素周期律及元素周期表的知识分析,下列关系中不正确的是( )
| A. | 酸性强弱:H3PO4>H2SO4>HClO4 | B. | 离子半径大小:F->Na+>Mg2+>Al3+ | ||
| C. | 稳定性大小:SiH4<PH3<H2S<HCl | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
10.化学与生活密切相关,下列说法中不正确的是( )
| A. | Al2O3 熔点高,可用于制作耐高温仪器 | |
| B. | 水果、蔬菜等是碱性食物 | |
| C. | 高纯度的硅单质可用于制作光导纤维 | |
| D. | 绿色化学的核心是从源头上杜绝污染的产生 |
11.有关该物质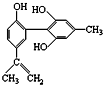 的说法正确的是( )
的说法正确的是( )
 的说法正确的是( )
的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 1 mol该物质分别与浓溴水和H2反应时,最多消耗Br2和H2分别为4 mol、7 mol |
