题目内容
6.某粗铜含铁、金和铅等杂质,通过电解精炼铜后,阳极泥含有Cu、Au(金)和PbSO4等杂质,为充分利用电解后的阳极泥和电解液,设计如下工艺流程:
回答下列问题:
(1)溶液A是一种绿色氧化剂,则反应①的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)试剂B为CuO或Cu(OH)2或CuCO3.
(3)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是将阳极泥粉碎,逆流焙烧等(写一点即可).
(4)操作Ⅰ的主要步骤为蒸发浓缩,降温结晶过滤,洗涤,干燥
(5)写出反应②的离子方程式2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+.
(6)为了减少废液排放、充分利用有用资源,工业上将滤液Ⅰ并入溶液Ⅰ进行循环操作,请指出流程图中另一处类似的做法用滤液Ⅱ溶解碱浸渣(或并入硝酸中).
(7)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)=1.2×10-8,用离子方程式表示加入碳酸钠溶液的作用PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
分析 粗铜精炼后的电解液中含有亚铁离子,加入溶液A是一种绿色氧化剂,应为双氧水,将亚铁离子氧化成铁离子,再调节PH值,得到氢氧化铁沉淀,阳极泥含有Cu、Au(金)和PbSO4等杂质,焙烧后金属铜成为氧化铜,酸浸可以得到硫酸铜溶液,硫酸铜溶液经过蒸发浓缩,降温结晶,过滤(或继续)洗涤,干燥获得硫酸铜晶体,酸浸渣含有Au(金)和PbSO4等经碳酸钠浸洗、浓硝酸氧化后,过滤得到硝酸铅溶液,滤液加硫酸生成硫酸铅沉淀,再过滤得到硫酸铅;脱铅滤渣主要是金,加王水溶金,得到含有AuCl4-的溶液,AuCl4-可以被SO2还原得到Au,
(1)反应①为亚铁离子被双氧水氧化成铁离子,根据电荷守恒和元素守恒书写离子方程式;
(2)试剂B目的是调节溶液的PH值,同时不能引入新杂质,据此判断;
(3)阳极泥的成分为Cu、Au(金)和PbSO4 等,在焙烧过程中铜被氧化为了CuO,根据阳极泥充分的粉碎,增大接触面积可以提高焙烧效率来回答;
(4)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,据此回答;
(5)反应②为SO2还原AuCl4-反应得到氧化产物是SO42-,还原产物是Au,配平书写方程式;
(6)将滤液1并入硫酸铜溶液进行循环操作,有利于充分利用,据此回答;
(7)碳酸铅比硫酸铅更加难溶,往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应.
解答 解:粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,焙烧后金属铜成为氧化铜,酸浸可以得到硫酸铜溶液,硫酸铜溶液经过蒸发浓缩,降温结晶,过滤(或继续)洗涤,干燥获得硫酸铜晶体;Au(金)和PbSO4等杂质经王水、浓硝酸氧化后可以得到硝酸铅以及含有AuCl4-+的物质,硝酸铅中加入硫酸可以转化为硫酸铅,AuCl4-可以被SO2还原得到Au.
(1)反应①为亚铁离子被双氧水氧化成铁离子,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(2)试剂B目的是调节溶液的PH值,同时不能引入新杂质,可以用CuO或Cu(OH)2或CuCO3,
故答案为:CuO或Cu(OH)2或CuCO3;
(3)要使焙烧效率提高,合理措施是把得到的阳极泥充分的粉碎,增大接触面积,或把反应后的气体在次逆流焙烧,这样可以升高温度且减少能耗,
故答案为:将阳极泥粉碎,逆流焙烧等;
(4)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,因此该步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤,
故答案为:蒸发浓缩,降温结晶;
(5)SO2还原AuCl4-中还原剂和氧化剂都比较明确,因此很容易推测出氧化产物是SO42-,还原产物是Au,根据氧化还原反应得失电子守恒先缺项配平,然后根据电荷守恒再配平,因此得到的反应方程式为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
故答案为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
(6)滤液Ⅰ是在结晶硫酸铜时剩下的滤液,还含有少量的未析出的硫酸铜,因此并入前面的硫酸铜溶液进行循环,有利于充分利用,因此类似此处的做法,应该是流程中得到的另一滤液Ⅱ,此滤液Ⅱ是在硝酸铅溶液中加入硫酸生成硫酸铅沉淀并过滤走硫酸铅后剩下的溶液,此溶液中H+没有发生反应,因此还有大量的硝酸溶液,所以可以把此滤液当成硝酸加入前面的碱浸渣中溶解碱浸渣,或者与前面碱浸渣步骤需要加入的硝酸合并加以利用,故答案为:用滤液Ⅱ溶解碱浸渣(或并入硝酸中);
(7)通过比较两种沉淀的溶度积,可以看出碳酸铅比硫酸铅更加难溶,因此往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应,离子方程式要注意标明状态,方程式为:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
故答案为:PbSO4(s)+CO32-(aq)?PbCO3(s)+SO42-(aq).
点评 本题考查混合物分离提纯,为高频考点,涉及物质的分离、离子的检验、电解原理、沉淀的转化等知识,把握实验流程及物质的性质为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度较大.

| A. | 石膏(CaSO4•2H2O) | B. | 硫铁矿(FeS2) | ||
| C. | 纯碱(NaHCO3) | D. | 芒硝(Na2SO4•10H2O) |
| A. | NO | B. | N2 | C. | N2O3 | D. | N2O5 |
| A. | 苯的分子式为C6H6 | B. | 乙烯的结构简式为CH2CH2 | ||
| C. | 四氯化碳的电子式: | D. | 硫离子结构示意图: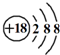 |
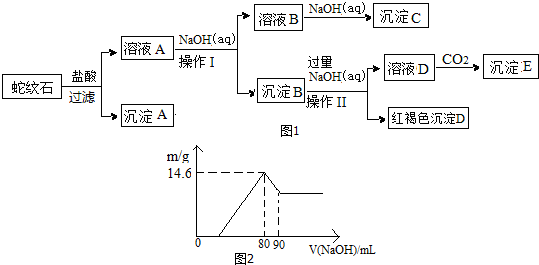
请回答下列问题:
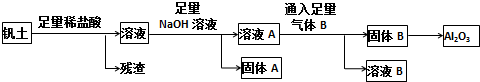
(1)蛇纹石与盐酸充分反应后再过滤即可得溶液A.在过滤中用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)沉淀B的组成是Al(OH)3、Fe(OH)3,向溶液A中逐滴加入NaOH溶液,以控制溶液pH在C的范围内可得到符合图1关系的沉淀B.(填写下列正确选项前的字母.有关氢氧化物沉淀的pH见下表,且pH达到7.8时,氢氧化铝开始溶解.)
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.9 | 3.3 | 9.4 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
(3)写出向溶液D中通入过量CO2反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
(4)向溶液A中逐滴加入5mol•mol-1NaOH溶液,经过操作I和操作II得到的沉淀质量与V[NaOH(aq)]有图2所示的数据关系.经分析蛇纹石中Fe2O3与Al2O3的物质的量之比为2:1.
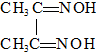 )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.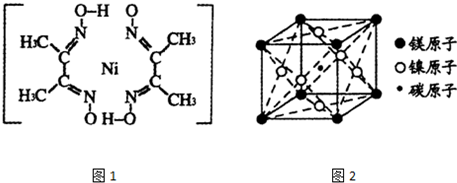
 .
.