题目内容
18.0.1L 2mol/L MgCl2溶液与0.4L 1mol/L AlCl3溶液中Cl-物质的量浓度比为4:3.分析 电解质溶液中离子浓度=电解质浓度×化学式中相应离子数目,溶液具有均一性,所以溶液浓度与体积无关.
解答 解:2mol/L的MgCl2溶液中Cl-的物质的量浓度为2mol/L×2=4mol/L,
1mol/L AlCl3溶液中Cl-物质的量浓度1mol/L×3=3mol/L,
所以:0.1L 2mol/L MgCl2溶液与0.4L 1mol/L AlCl3溶液中Cl-物质的量浓度比为:4:3;
故答案为:4:3.
点评 本题考查物质的量浓度计算,比较基础,注意根据电解质的电离理解电解质离子与电解质溶液浓度关系,注意溶液具有均一性,所以溶液浓度与体积无关.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
8.某溶液中含有Ba2+、Ag+、Cu2+三种离子,现用①NaOH溶液;②K2SO4溶液;③HCl将这三种离子逐一沉淀并加以分离,则加入试剂顺序正确的是( )
| A. | ①②③ | B. | ③②① | C. | ②③① | D. | ①③② |
10.在有机化合物中,一个碳原子与其他原子不能同时形成的化学键是( )
| A. | 四个共价单键 | B. | 一个双键,一个三键 | ||
| C. | 两个单键,一个双键 | D. | 一个单键,一个三键 |
7.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 在常温常压下,46g NO2和N2O4混合气体所含氧原子数目为2NA | |
| C. | 将1L 2mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
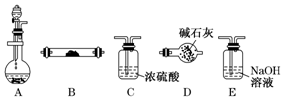 如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.
如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.