题目内容
6.某工业废液里含有FeCl2、CuCl2和FeCl3.为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程: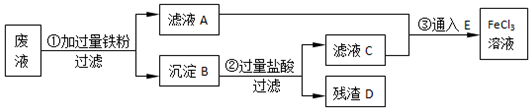
(1)A的化学式为FeCl2,E的化学式为Cl2.
(2)B的化学成份Fe、Cu,回收的铜是D(填A、B、C、D或E).
(3)根据图示,反应②的化学方程式为Fe+2HCl=FeCl2+H2↑.
分析 由流程图可知废液的处理过程为:工业废液里含有FeCl2、CuCl2和FeCl3.用过量铁粉把生成的氯化铜置换得到金属铜,同时把过量的氯化铁溶液转变为氯化亚铁溶液,过滤所得沉淀B为铁和铜,用过量盐酸溶解铁后分离铜和铁,残渣D为Cu,最后,进行过滤分离出金属铜而回收铜,滤液C为氯化亚铁溶液,最后,进行过滤分离出金属铜而回收铜,并把滤液A和滤液C为氯化亚铁溶液合并,通入E为氯气,氯化亚铁与氯气反应而转化为氯化铁溶液循环利用.
解答 解:(1)反应后的滤液A为FeCl2,E为Cl2,故答案为:FeCl2;Cl2;
(2)CuCl2和FeCl3中加入铁粉,分别发生:Fe+2FeCl3=3FeCl2,Fe+CuCl2=Cu+FeCl2,B的化学成份为Fe、Cu,回收的铜是D,
故答案为:Fe、Cu;D;
(3)Fe比Cu活泼,可与盐酸反应生成而分离出Cu,反应②的化学方程式为:Fe+2HCl=FeCl2+H2↑,
故答案为:Fe+2HCl=FeCl2+H2↑.
点评 本题考查物质的分离,题目难度中等,注意根据流程结合物质的性质解答该题.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
17.下列叙述正确的是( )
| A. | 氢氧化钠的摩尔质量是40 g | |
| B. | 1 mol NaOH的质量是40 g/mol | |
| C. | 1gH2和lgN2含分子数相等 | |
| D. | 等质量的N2、CH4、CO、H2O中,CH4含分子数最多 |
14.X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
请回答下列问题:
(1)W元素在周期表中的位置第三周期第VIIA族.
(2)X、Y、Z、W分别形成的简单离子的半径由小到大的顺序为O2-<N3-<Cl-<S2-(用化学式填写,下同);Y、Z对应的气态氢化物的稳定性H2O>H2S.
(3)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式为2SO2(g)+O2(g)?2SO3(g)△H=-190.0kJ•mol-1.
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O=SO2+3S+4HCl.
| X | Y | |
| Z | W |
(1)W元素在周期表中的位置第三周期第VIIA族.
(2)X、Y、Z、W分别形成的简单离子的半径由小到大的顺序为O2-<N3-<Cl-<S2-(用化学式填写,下同);Y、Z对应的气态氢化物的稳定性H2O>H2S.
(3)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式为2SO2(g)+O2(g)?2SO3(g)△H=-190.0kJ•mol-1.
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O=SO2+3S+4HCl.
11.某烃的结构简式如下: 分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )
分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )
 分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )
分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c.则a、b、c分别为( )| A. | 4、4、7 | B. | 4、3、6 | C. | 3、5、4 | D. | 2、6、4 |
15.在容积一定的密闭容器中,可逆反应A(g)+B(g)?xC(g),有如图所示的关系曲线,根据下图下列判断正确的是( )
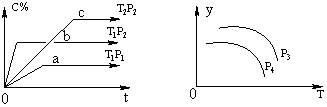

| A. | p3>p4,y轴表示A的物质的量分数 | |
| B. | 若增大A的浓度,平衡体系颜色加深,C一定是有颜色的气体 | |
| C. | p3<p4,y轴表示平衡常数K | |
| D. | p3>p4,y轴表示混合气体的平均摩尔质量 |
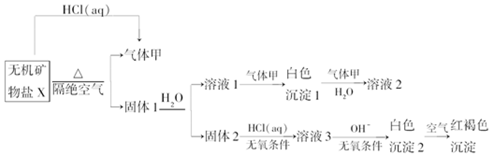
 ,写出气体甲的电子式
,写出气体甲的电子式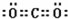 .
.