题目内容
1.分子式为C5H11Cl的有机物的同分异构体有( )| A. | 5 | B. | 8 | C. | 9 | D. | 10 |
分析 先确定C5H12的同分异构体:正戊烷、异戊烷和新戊烷,然后根据各有机物的结构简式及等效H原子分别判断正戊烷、异戊烷和新戊烷中含有的一氯代物种类即可.
解答 解:分子式为C5H11Cl的同分异构体有:
主链有5个碳原子的一氯代物为:CH3CH2CH2CH2CH2Cl、CH3CH2CH2CHClCH3、CH3CH2CHClCH2CH3;
主链有4个碳原子的一氯代物为:CH3CH(CH3)CH2CH2Cl、CH3CH(CH3)CHClCH3、CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;
主链有3个碳原子的一氯代物为:CH2C(CH3)2CH2Cl,
根据分析可知,C5H11Cl的同分异构体总共有8种,
故选B.
点评 本题考查同分异构体的判断,难度不大,做题时要抓住判断角度,找出等效氢原子种类.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 在常温常压下,11.2LN2所含有的原子数目为NA | |
| B. | 活泼金属从盐酸中置换出1molH2,电子转移的数目为NA | |
| C. | 500mL0.5 mol/L的硫酸铝溶液中,硫酸根离子的浓度为1.5 mol/L | |
| D. | 1.7克氨气所含有的电子数目为10 NA |
12.下列有关离子共存或离子反应的说法,正确的是( )
| A. | 与Al反应能放出H2的溶液中可能大量存在Fe2+、Na+、NO3-、Cl- | |
| B. | 使紫色石蕊变蓝的溶液中可能大量存在Al3+、SO42-、NH4+、CO32- | |
| C. | Al2(SO4)3溶液与氨水的反应:Al3++3OH-=Al(OH)3↓ | |
| D. | FeCl3溶液腐蚀印刷电路板的反应:2Fe3++Cu=2Fe2++Cu2+ |
9.下列各选项中所述的两个量,前者比后者大的是( )
| A. | 25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度 | |
| B. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 | |
| C. | 物质的量浓度相等的(NH4)2SO4溶液和(NH4)2SO3溶液中NH4+的浓度 | |
| D. | 将pH=4的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量 |
6.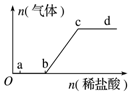 向Na2CO3、NaHCO3混合溶液中逐滴滴入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴滴入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴滴入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴滴入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液中:Al3+、H+、SO42-、NO3- | |
| B. | b点对应的溶液中:Ca2+、Na+、OH-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:F-、NO3-、Fe3+、Na+ |
13.化学与生产、生活密切相关.下列说法正确的是( )
| A. | 明矾净水原理不涉及化学变化 | |
| B. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说明“纳米铜”的还原性比铜片更强 |
10.有两种不同的原子团-X、-Y,若同时分别取代甲苯苯环上的两个氢原子,生成的同分异体的数目是( )
| A. | 8种 | B. | 10种 | C. | 16种 | D. | 20种 |