题目内容
15.战国时成书的《尚书•洪范篇》有“稼稿作甘”之句,“甘”即饴糖,饴糖的主要成分是一种双糖,1mol该双糖完全水解可生成2mol葡萄糖.饴糖的主要成分是( )| A. | 淀粉 | B. | 蔗糖 | C. | 果糖 | D. | 麦芽糖 |
分析 1mol麦芽糖完全水解可生成2mol葡萄糖,据此解题.
解答 解:1mol麦芽糖完全水解可生成2mol葡萄糖,糖的主要成分是麦芽糖.
故选D.
点评 本题考查糖类的水解,难度不大,掌握糖类水解方程式的书写是解题的关键.

练习册系列答案
相关题目
5.有反应方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O,当32gCu完全反应时,被还原的H2SO4的物质的量为(已知:MCu=64g/mol)( )
| A. | 0.5mol | B. | 1.0mol | C. | 1.5mol | D. | 2.0mol |
3.某同学取不同质量的镁铝合金样品分别与30mL同浓度的盐酸反应,所取合金质量与产生气体体积(已转化为标准状况)如下:
通过计算求:
(1)该盐酸的物质的量浓度?
(2)合金中镁的质量分数?
(3)在c组实验后,还需向容器中加入多少毫升同浓度的盐酸才能使剩余合金恰好完全溶解?
| 实验序号 | a | b | c |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
(1)该盐酸的物质的量浓度?
(2)合金中镁的质量分数?
(3)在c组实验后,还需向容器中加入多少毫升同浓度的盐酸才能使剩余合金恰好完全溶解?
10.已知反应2NO2(g)?N2O4(g)△H<0,在100℃时,将0.400mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
下列分析合理的是( )
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.08 | 0.08 |
| A. | 从反应开始直至60s和80s时,二氧化氮的平均反应速率是相等的 | |
| B. | 80s后将容器的体积缩小为1L,平衡向正反应方向移动,气体颜色变浅 | |
| C. | n1的范围是0.28<n1<0.33 | |
| D. | 升高温度,既能加快反应速率,也能提高N2O4的体积分数 |
7.为了除去混入CO2中的SO2和O2,下列试剂的使用顺序正确的是( )
①饱和的Na2CO3溶液 ②饱和的NaHCO3溶液 ③浓硫酸 ④灼热的铜网 ⑤碱石灰.
①饱和的Na2CO3溶液 ②饱和的NaHCO3溶液 ③浓硫酸 ④灼热的铜网 ⑤碱石灰.
| A. | ①③④ | B. | ②③④ | C. | ②④⑤ | D. | ③④⑤ |
4.实验室中下列药品的保存方法,正确的是( )
| A. | 氢氟酸保存在玻璃瓶中 | B. | 金属钠保存在煤油中 | ||
| C. | 氧化钠保存在敞口容器中 | D. | 浓硫酸保存在橡胶塞试剂瓶中 |
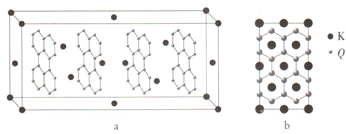 Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子.
Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子.