��Ŀ����
6��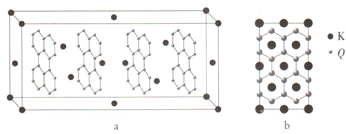 Q��R��X��Y��Z��ԭ���������������ǰ������Ԫ�أ�Q��һ�ֵ�������Ȼ���ڵ���Ӳ�����ʣ�Xԭ�ӵĺ�������а����˶�״̬��YԪ�ص����Ӱ뾶�ǵ�����������С�ģ�Z�ǵ���������δ�ɶԵ�������ԭ�ӣ�
Q��R��X��Y��Z��ԭ���������������ǰ������Ԫ�أ�Q��һ�ֵ�������Ȼ���ڵ���Ӳ�����ʣ�Xԭ�ӵĺ�������а����˶�״̬��YԪ�ص����Ӱ뾶�ǵ�����������С�ģ�Z�ǵ���������δ�ɶԵ�������ԭ�ӣ���1��Zԭ�ӵļ۵����Ų�ʽΪ3d54s1��
��2��Q��R��X��Y����Ԫ�صĵ縺���ɴ�С��˳����O��N��C��Al��
��3���ӻ��������ָ��ԭ�������������s��p��s��p��d���֮�����ͨ���ӻ��γ�����ḻ���ӻ������RCl3��������ԭ�ӵ��ӻ���ʽΪsp3����ԭ�ӽṹ�ĽǶȽ��Ͳ�����RCl5���ӵ�ԭ��Nԭ�ӵ������ֻ��2s��2p��4�ʹ����û��d��������γ�NCl5��
��4�������ķ���ʽΪZCl3•4H2O����λ��Ϊ6��ȡ1mol������ˮ������������AgNO3��Һ���õ�143.5g��ɫ��������������Һ�У�����ˮ�Ϸ�Ӧת��Ϊ�ң�ZCl3•6H2O�����ҵ���λԭ��ֻ��һ�֣���λ��Ϊ6��
�ټĽṹ��ʽΪ[Cr��H2O��4Cl2]Cl��
�ڼס��ҵĻ�ѧ����ʽΪ[Cr��H2O��4Cl2]Cl+2H2O$\frac{\underline{\;H+\;}}{\;}$[Cr��H2O��6]Cl3 ��
��5��ͼa��Q��һ��ͬ��������ͼ��γɵIJ�㻯����ľ���ͼ��ͼb�Ǿ����ز����ͶӰͼ���ò�㻯����Ļ�ѧʽΪKC8��
���� Q��R��X��Y��Z��ԭ���������������ǰ������Ԫ�أ�Q��һ�ֵ�������Ȼ���ڵ���Ӳ�����ʣ���QΪCԪ�أ�Xԭ�ӵĺ�������а����˶�״̬����XΪOԪ�أ�R��ԭ����������̼����֮�䣬��RΪNԪ�أ�YԪ�ص����Ӱ뾶�ǵ�����������С�ģ���YΪAl��Z�ǵ���������δ�ɶԵ�������ԭ�ӣ���Zԭ����Χ�����Ų�ʽΪ3d54s1����ZΪCr��
��� �⣺Q��R��X��Y��Z��ԭ���������������ǰ������Ԫ�أ�Q��һ�ֵ�������Ȼ���ڵ���Ӳ�����ʣ���QΪCԪ�أ�Xԭ�ӵĺ�������а����˶�״̬����XΪOԪ�أ�R��ԭ����������̼����֮�䣬��RΪNԪ�أ�YԪ�ص����Ӱ뾶�ǵ�����������С�ģ���YΪAl��Z�ǵ���������δ�ɶԵ�������ԭ�ӣ���Zԭ����Χ�����Ų�ʽΪ3d54s1����ZΪCr��
��1��ZΪCrԪ�أ�ԭ�ӵļ۵����Ų�ʽΪ3d54s1���ʴ�Ϊ��3d54s1��
��2��ͬ����������ҵ縺������ͬ�������϶��µ縺�Լ�С���ʵ縺�ԣ�O��N��C��Al��
�ʴ�Ϊ��O��N��C��Al��
��3��NCl3����Nԭ���γ�3��N-Cl��������1�Թ¶Ե��ӣ��ӻ������ĿΪ4��Nԭ�Ӳ�ȡsp3�ӻ���Nԭ�ӵ������ֻ��2s��2p��4�ʹ����û��d��������γ�NCl5��
�ʴ�Ϊ��sp3��Nԭ�ӵ������ֻ��2s��2p��4�ʹ����û��d��������γ�NCl5��
��4�������ķ���ʽΪCrCl3•4H2O����λ��Ϊ6��ȡ1mol������ˮ������������AgNO3��Һ���õ�143.5g��ɫ����ΪAgCl�������ʵ���Ϊ1mol������1��Cl-������磬2��Cl-�����ڽ磬��Ļ��ṹ��ʽΪ��[Cr��H2O��4Cl2]Cl����������Һ�У�����ˮ�Ϸ�Ӧת��Ϊ�ң�ZCl3•6H2O�����ҵ���λԭ��ֻ��һ�֣���λ��Ϊ6������Ϊ[Cr��H2O��6]Cl3���ס��ҵĻ�ѧ����ʽΪ��[Cr��H2O��4Cl2]Cl+2H2O$\frac{\underline{\;H+\;}}{\;}$[Cr��H2O��6]Cl3 ��
�ʴ�Ϊ��[Cr��H2O��4Cl2]Cl��[Cr��H2O��4Cl2]Cl+2H2O$\frac{\underline{\;H+\;}}{\;}$[Cr��H2O��6]Cl3 ��
��5��������Kԭ����ĿΪ4+8��$\frac{1}{8}$+6��$\frac{1}{2}$=8��Cԭ����ĿΪ12��4+8��$\frac{1}{2}$��4=64��K��Cԭ����Ŀ֮��Ϊ8��64=1��8���ʸò�㻯����Ļ�ѧʽ��KC8��
�ʴ�Ϊ��KC8��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų����縺�ԡ��ӻ�������������������ȣ���4��ע���ڽ�����粻ͬ����5����Ҫѧ���߱�һ���Ŀռ�����Ͼ�̯�����㣮

 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�| A�� | �۱�ϩ��������-CH2-CH2-CH2- | |
| B�� | ����Һ�еμ�Na2CO3��Һ��2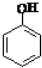 +CO${\;}_{3}^{2-}$�� +CO${\;}_{3}^{2-}$��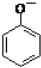 +CO2��+H2O +CO2��+H2O | |
| C�� | 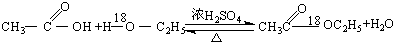 | |
| D�� | ����ͬϵ����ʹ���Ը��������Һ��ɫ��˵�������Ա��������ʲ����˽ϴ��Ӱ�� |
 ����ʱ����100mL 0.1mol/L NH4HSO4��Һ�еμ�0.1mol/L NaOH��Һ���õ���ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��
����ʱ����100mL 0.1mol/L NH4HSO4��Һ�еμ�0.1mol/L NaOH��Һ���õ���ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ��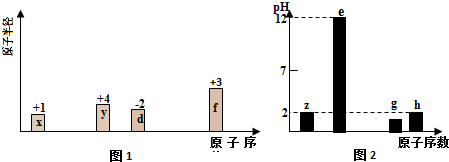
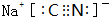 ��
��