题目内容
3.氢气、碳、辛烷、甲烷的热化学方程式分别为:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ•mol-1
C(s)+$\frac{1}{2}$O2(g)═CO (g);△H=-111.0kJ•mol-1
C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l);△H=-5518kJ•mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ•mol-1
其中反应热能表示该物质燃烧热的是( )
| A. | C8H18 | B. | CH4 | C. | H2 | D. | C |
分析 燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物以此解答该题.
解答 解:氢气的物质的量不是1mol,△H不代表燃烧热,故错误;
生成的氧化物CO产物,不是稳定氧化物,△H不代表燃烧热,故错误;
C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l);△H=-5518kJ•mol-1,符合燃烧热概念,故正确;
水的状态为气态,产物为不是稳定氧化物,△H不代表燃烧热,故错误;
故选A.
点评 本题考查了燃烧热的概念,题目难度不大,解题时注意燃烧热的热化学方程式中,可燃物为1mol,产物为稳定氧化物.

练习册系列答案
相关题目
14.下列实验操作中,正确的是( )
| A. | 在蒸发食盐水时,边加热边用玻璃棒搅拌直至液体蒸干 | |
| B. | 鉴别Na2CO3与NaHCO3固体可用加热的方法 | |
| C. | 实验室制备氢氧化铁胶体时,向饱和氯化铁溶液中滴加氢氧化钠溶液 | |
| D. | 配制一定物质的量浓度的NaOH溶液,将NaOH固体放在容量瓶中加水溶解 |
18.下列关于庚烷的同分异构体说法正确的是( )
| A. | 主链上有6个碳的庚烷有3种 | |
| B. | 主链4个碳,可能只含一个支链 | |
| C. | 主链5个碳,支链可以只含乙基,也可以只含甲基 | |
| D. | 主链为3个碳时,支链形成的同分异构体含两个乙基支链,碳架结构为: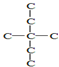 |
8.下列溶液中Cl-浓度最大的是( )
| A. | 2 mol•L-1的HCl溶液 | B. | 1 mol•L-1的KCl溶液 | ||
| C. | 0.8 mol•L-1的AlCl3溶液 | D. | 0.5 mol•L-1的FeCl2溶液 |
15.从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
| A. | 2NaBr+Cl2=2CaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2=2H2O+3S↓ | |
| D. | 2CO+O2=2CO2 |
13.有机物种类繁多的原因的主要原因( )
| A. | 有机物分子结构十分复杂 | |
| B. | 自然界中存在着多种形式的大量的有机物 | |
| C. | 碳原子能与其他原子形成四个共价键,且碳原子间也可以成键,而且有同分异构现象 | |
| D. | 有机物除含碳元素之外,还含有其他多种元素 |
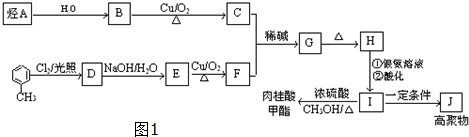
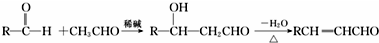
 $→_{△}^{硫酸}$
$→_{△}^{硫酸}$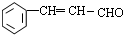 +H2O.
+H2O.