题目内容
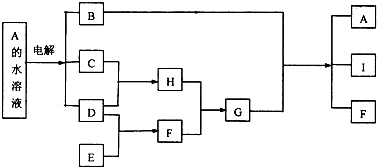
17.A、B、C、D均为中学学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):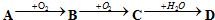
(1)若A能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红,则A为NH3,C物质的颜色红棕色写出A→B转化的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(2)若A为活泼金属元素的单质,焰色反应显黄色,D为强碱,则C是Na2O2.C跟水发生反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.
(3)若A为常见的淡黄色固体单质,则A是S,B是SO2,
若将B 气体与H2S气体反应则会发现有淡黄色物质产生,原因是(用化学反应方程式表示)2H2S+SO2=3S+2H2O如何检验某溶液中是否含有D中的阴离子?:取少量于试管中滴入盐酸无现象,加入氯化钡溶液生成白色沉淀证明含有硫酸根离子,.
分析 (1)根据使湿润的红色石蕊试纸变蓝确定A是氨气,B为NO,C为NO2,进而确定D是硝酸;
(2)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则A为Na、B为Na2O、C为Na2O2、D为NaOH,过氧化钠和水反应生成氢氧化钠和氧气;
(3)根据颜色确定A为S,根据一系列反应得出D为硫酸,即说明A是S,则B是二氧化硫,C是三氧化硫,D是硫酸,若将B 气体与H2S气体反应则会发现有淡黄色物质产生,是二氧化硫和硫化氢反应生成硫单质和水,检验某溶液中是否含有D中的阴离子是检验硫酸根离子的存在.
解答 解:(1)A的水溶液能使湿润的红色石蕊试纸变蓝,说明A是氨气,则B是一氧化氮,C是二氧化氮,D是硝酸.由氨气制得一氧化氮,是氨气的催化氧化,C为二氧化氮为红棕色气体,即4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:NH3;红棕色,4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(2)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则A为Na、B为Na2O、C为Na2O2、D为NaOH,钠跟水发生反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,
故答案为:Na2O2;2Na2O2+2H2O═4NaOH+O2↑.
(3)常温下A为淡黄色固体单质,即说明A是S,则B是二氧化硫,C是三氧化硫,D是硫酸,若将B 气体与H2S气体反应则会发现有淡黄色物质产生,是二氧化硫和硫化氢反应生成硫单质和水,反应的化学方程式为:2H2S+SO2=3S+2H2O,检验某溶液中是否含有D中的阴离子是检验硫酸根离子的存在,可以取少量于试管中滴入盐酸无现象,加入氯化钡溶液生成白色沉淀证明含有硫酸根离子,
故答案为:S;SO2;2H2S+SO2=3S+2H2O;取少量于试管中滴入盐酸无现象,加入氯化钡溶液生成白色沉淀证明含有硫酸根离子;
点评 本题考查无机物推断,侧重于学生的分析能力的考查,需要学生熟练掌握元素化合物知识,注意掌握中学常见连续氧化反应,物质性质的熟练掌握是解题关键,题目较简单.

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案| A. | 常温下SO3是液体 | |
| B. | 标准状况下,1 mol SO3的体积约为22.4L | |
| C. | SO3与CaO反应生成CaSO3 | |
| D. | SO2遇空气即生成SO3 |
①适量的盐酸 ②适量的NaCl ③适量的醋酸 ④适量的CH3COONa.
| A. | ①② | B. | ③ | C. | ③④ | D. | ④ |
| A. | 某溶液$\stackrel{+AgNO_{3}溶液}{→}$生成白色沉淀,说明原溶液中含有Cl- | |
| B. | 某溶$\stackrel{+HCl溶液}{→}$无现象$\stackrel{+BaCl_{2}溶液}{→}$生成白色沉淀,+说明原溶液中含有SO42- | |
| C. | 某溶$\stackrel{+NaOH溶液}{→}$生成红褐色沉淀,说明原溶液中含有Fe3+ | |
| D. | 某溶$\stackrel{+稀硫酸}{→}$生成无色气体,说明原溶液中含有CO32- |
| A | B | C | D |
| NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾[KAl(SO4)2•12H2O]溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
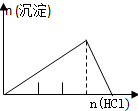 | 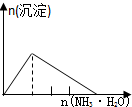 | 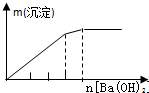 | 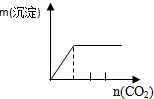 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
| A. | HNO3溶液 | B. | Ba(OH)2溶液 | C. | H2SO4溶液 | D. | HCl溶液 |
(1)制取H2和CO通常采用:C(s)+H2O(g)═CO(g)+H2(g)△H=+131.4kJ•mol-1,下列判断正确的是AD.
A.该反应的反应物总能量小于生成物总能量
B.标准状况下,上述反应生成ILH2气体时吸收131.4kJ的热量
C.若CO(g)+H2(g)═C(s)+H2O(l)△H=-QkJ•mol-1,则Q<131.4
D.若C(s)+CO2(g)═2CO(g)△H1;CO(g)+H2O(g)═H2(g)+CO2(g)△H2 则:△H1+△H2=+131.4kJ•mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO.该反应为:CH4(g)+H2O(g)═CO(g)+3H2(g)
己知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
| 不同时间各物质的物质的量/mol | ||||
| 0min | 2min | 4min | 6min | |
| CH4 | 2.00 | 1.76 | 1.60 | n2 |
| H2 | 0.00 | 0.72 | n1 | 1.20 |
①0min~2min内H2的平均反应速率为0.18mol•L-1•min-1.
②达平衡时,CH4的转化率为20%.在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比变小(填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有ad(填字母)
A.CO的含量保持不变 B.容器中c(CH4)与c(CO)相等
C.容器中混合气体的密度保持不变 D.3v正(CH4)=v逆(H2)
( 3 )合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的.工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过).

①a电极的名称为阳极.
②写出除去甲醇的离子方程式6Co3++CH3OH+H2O=6Co2++CO2+6H+.
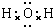 ;
;