题目内容
9.某无色透明溶液可能含有下列离子中的一种或几种:Na+、Cu2+、Mg2+、OH-、Cl-、CO32-、NO3-.现进行如下实验:①用红色石蕊试纸检验,试纸变蓝
②另取少量溶液逐滴加盐酸至过量,无气体放出.
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成.
(1)根据上述实验推断:原溶液中肯定有OH-、Na+、Cl-离子,肯定没有Mg2+、Cu2+、CO32-离子,不能肯定存在NO3- 离子.
(2)操作③的离子方程式是Cl-+Ag+═AgCl↓.
分析 (1)无色透明溶液,说明溶液中不含Cu2+,据①得出此溶液显碱性;
据②得出此溶液中不含有CO32-;
据③得出溶液中含有Cl-,据此解答即可;
(2)操作③的离子方程式是:Cl-+Ag+═AgCl↓.
解答 解:(1)无色透明溶液,说明溶液中不含Cu2+,用红色石蕊试纸检验,试纸变蓝色,故此溶液显碱性,故含有OH-,此时判断一定不能含有Mg2+;
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,故此溶液一定不含有CO32-;
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成,此白色沉淀为AgCl,故此溶液中一定含有Cl-,到此不能确定的离子是NO3-,溶液呈电中性,根据电荷守恒一定有阳离子钠离子;
故答案为:OH-、Na+、Cl-; Mg2+、Cu2+、CO32-; NO3-;
(2)操作③的离子方程式是:Cl-+Ag+═AgCl↓,故答案为:Cl-+Ag+═AgCl↓.
点评 本题主要考查了根据实验现象判断离子共存,要掌握根据实验现象判断存在的离子,排除与该离子反应的离子.

练习册系列答案
相关题目
16.维生素C的结构简式为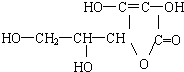 ,有关它的叙述错误的是( )
,有关它的叙述错误的是( )
 ,有关它的叙述错误的是( )
,有关它的叙述错误的是( )| A. | 在碱性溶液中能稳定地存在 | B. | 易起氧化及加成反应 | ||
| C. | 可以溶解于乙醇 | D. | 是一个环状的酯类化合物 |
20.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 标准状况下,2.24 L Cl2与足量的稀NaOH溶液反应,转移电子总数为0.2 NA | |
| B. | 欲配制1.00 L 1.00 mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 | |
| C. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| D. | 标准状况下,0.1NA的SO3的体积约为2.24 L |
17.四个体积相同的密闭容器,在一定条件下,发生如下反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3,化学反应速率最快的是( )
| 容器 | 温度(℃) | H2(mol) | N2(mol) | 催化剂 |
| A | 450 | 3 | 1 | 无 |
| B | 450 | 3 | 1 | 有 |
| C | 500 | 6 | 2 | 有 |
| D | 500 | 6 | 2 | 无 |
| A. | A | B. | B | C. | C | D. | D |
1.下列关于糖类、蛋白质、油脂的说法中,正确的是( )
| A. | 它们的组成元素中都有C、H、O、N等元素 | |
| B. | 在一定条件下,它们都能发生水解反应 | |
| C. | 人体需要的二十多种氨基酸都可以通过人体自身合成 | |
| D. | 油脂分为油和脂肪,它们都是高级脂肪酸的甘油酯 |
19.鉴别KCl、KBr、KI三种溶液选用的试剂为( )
| A. | CCl4 | B. | AgNO3溶液 | C. | 溴水 | D. | 淀粉溶液 |