题目内容
7.实验室用30%左右的硫酸溶液(约3.7mol•L-1)与锌粒反应制取氢气.下列措施中不可能加快反应速率的是( )| A. | 适当升高温度 | |
| B. | 将锌粒改为锌粉 | |
| C. | 将所用硫酸改为98%左右的硫酸溶液 | |
| D. | 寻找一种合适的催化剂并加入其中 |
分析 增大金属与酸反应的化学反应速率,可通过增大浓度、升高温度或形成原电池反应等措施,注意浓硫酸和铁发生钝化反应.
解答 解:A.升高温度,增大活化分子百分数,反应速率增大,故A不选;
B.用锌粉代替锌粒,固体表面积增大,反应速率增大,故B不选;
C.将所用硫酸改为98%左右的硫酸溶液,发生氧化反应生成二氧化硫,不是生成氢气,故C选;
D.加入催化剂,增大活化分子百分数,反应速率增大,故D不选.
故选C.
点评 本题考查影响反应速率的因素,为高频考点,把握温度、浓度、原电池对反应速率的影响即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
17.化学与人类生活、生产和社会可持续发展密切相关,下列说法正确的是( )
| A. | 为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 铝及其合金是电气、工业、家庭广泛使用的材料,通常用电解氯化铝的方法制取铝 | |
| D. | DNOP(邻苯二甲酸二辛酯)是一种由邻苯二甲酸和正辛醇经酯化反应而得的一种酯类有机化合物,常用作增塑剂、溶剂以及气相色谱固定液,对人体无害,可用作食品添加剂 |
18.短周期元素X和Y,可组成化合物XY 3,当X的原子序数为m,Y的原子序数可能是( )
①m+4 ②m-4 ③m-8 ④m+2⑤m-6 ⑥m+12.
①m+4 ②m-4 ③m-8 ④m+2⑤m-6 ⑥m+12.
| A. | ①②③ | B. | ①④⑤⑥ | C. | ①②③④⑤ | D. | ①②③④⑤⑥ |
12.X、Y是元素周期表ⅦA族中的两种元素,X的非金属性比Y的强.则下列叙述中,正确的是( )
| A. | X原子的电子层数比Y原子的电子层数多 | |
| B. | X的单质一定能将Y从NaY的水溶液中置换出来 | |
| C. | X的单质比Y的单质更容易与氢气反应 | |
| D. | X的氢化物水溶液的酸性一定比Y的氢化物水溶液的酸性强 |
16.铜是一种紫红色金属,被称作“电器工业的主角”铜主要是黄铜矿炼制,焙烧时发生反应2CuFeS2+O2$\frac{\underline{\;高温\;}}{\;}$Cu2S+2FeS+SO2,其简单流程如图所示,下列说法正确的是( )
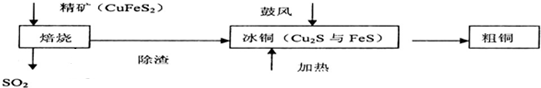

| A. | 焙烧时硫元素全部转化为二氧化硫 | B. | 在焙烧时氧化剂只有氧气 | ||
| C. | 粗铜精炼时用粗铜做阴极 | D. | Cu2S可用于火法炼制铜 |