题目内容
6.有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图1所示: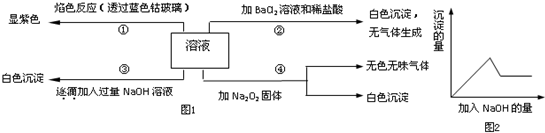
第③个实验中,生成白色沉淀的量与加入NaOH的量有图2所示的相互关系.据此可知:
(1)原溶液中一定不存在的离子有Fe3+、Fe2+、Cu2+、CO32-;
(2)满足该溶液中一定存在的离子的要求,一般可溶解两种常见物质(写化学式)KAl(SO4)2和MgSO4在溶液中.
(3)写出第③个实验中发生反应的离子方程式Mg2++2OH-=Mg(OH)2;Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-═AlO2-+2H2O.
分析 溶液透过蓝色钴玻璃焰色反应呈紫色,说明溶液中含有K+离子,溶液呈无色,则一定不含有色离子,逐滴加入过量NaOH溶液有白色沉淀,则溶液中含有Mg2+离子;加入氯化钡和盐酸后生成白色沉淀,由于溶液中没有Ag+离子,则生成沉淀为BaSO4,溶液中含有SO42-离子,第③个实验中,生成白色沉淀的量与加入NaOH的量的先增大后减小,则说明溶液中含有Al3+离子,据此进行解答.
解答 解:透过蓝色钴玻璃焰色反应呈紫色,说明溶液中含有K+离子;溶液呈无色,则一定不含有色离子:Fe3+、Fe2+、Cu2+;逐滴加入过量NaOH溶液有白色沉淀,则溶液中含有Mg2+离子,一定不含CO32-;加入氯化钡和盐酸后生成白色沉淀,由于溶液中没有Ag+离子,则生成沉淀为BaSO4,溶液中含有SO42-离子,第③个实验中,根据图象可知:生成白色沉淀的量与加入NaOH的量的先增大后减小,最后不再变化,则说明溶液中含有Al3+离子,一定不含有铵根离子,综上可知:原溶液中一定含有Al3+、Mg2+、K+、SO42-,一定不含Fe3+、Fe2+、NH4+、Cu2+、CO32-,
(1)根据以上分析可知,原溶液中一定不含有:Fe3+、Fe2+、NH4+、Cu2+、CO32-,
故答案为:Fe3+、Fe2+、NH4+、Cu2+、CO32-;
(2)原溶液中一定含有的离子为:Al3+、Mg2+、K+、SO42-,可以组成的物质为:KAl(SO4)2(或KAl(SO4)2•12H2O)、MgSO4,
故答案为:KAl(SO4)2(或KAl(SO4)2•12H2O);MgSO4;
(3)溶液中含有Al3+、Mg2+,加入氢氧化钠发生的反应有:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Mg2++2OH-=Mg(OH)2↓;Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查了未知物的推断、常见离子的检验,题目难度中等,正确根据反应现象推断存在的离子为解答本题的关键,注意掌握离子的特征反应,如铝离子与氢氧化钠溶液的反应现象.

 步步高达标卷系列答案
步步高达标卷系列答案| A. | 二氯化氧(OCl2) | B. | 次氯酸(HClO) | C. | 三氟化硼(BF3) | D. | 六氟化氙(XeF6) |
①取l0mL该溶液于试管中滴加足量的Ba(N03)2溶液,加稀硝酸酸化后过滤得到0.03mol
白色沉淀甲.
②取上述反应后的滤液,加人AgN03溶液未见沉淀产生.
③另取l0mL该溶液于试管中,滴加NaOH溶液产生白色沉淀乙,当加人NaOH的物质的量为0.03mol时,沉淀的量达到最大;继续滴加NaOH溶液并加热,开始产生气体丙,收集气体丙,体积换算成标况下为0.224L(假设丙全部逸出),最后沉淀完全溶解.
下列推断正确的是( )
| A. | 肯定有Na+、Al3+、Mg2+、SO42- | B. | 肯定有Na+、Mg2+、Al3+、Cl- | ||
| C. | 肯定没有Mg2+、HCO3-、MnO4-、Cl- | D. | 肯定没有K+、NH4+、Cl- |
 ,则A的结构简式为
,则A的结构简式为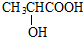 .
.