题目内容
17.下列有关有机化合物的叙述正确的是( )| A. | 植物油与聚乙烯均能使溴水褪色 | |
| B. | 淀粉与纤维素均为高分子化合物且互为同分异构体 | |
| C. | 蔗糖与麦芽糖的水解产物均为葡萄糖 | |
| D. | 丙烷与2-甲基丙烷的一氯代物均为两种 |
分析 A.聚乙烯不含不饱和键;
B.淀粉纤维素的分子式不同;
C.蔗糖水解生成葡萄糖和果糖;
D.根据等效氢原子的种类判断.
解答 解:A.聚乙烯不含不饱和键,不能使溴水褪色,故A错误;
B.淀粉(C6H10O5)n.和纤维素(C6H10O5)n.虽有相同的表示式,但n不同,所以分子式不同,结构也不相似,所以不是同分异构体,故B错误;
C.蔗糖水解生成葡萄糖和果糖,故C错误;
D.丙烷中含有2种H,2-甲基丙烷中也含有2种H,故丙烷和2-甲基丙烷的一氯代物均为两种,故D正确.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重常见有机物性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
7.下列物质在空气里完全燃烧,生成二氧化碳和水的物质的量之比为1:1的有( )
| A. | 甲醇 | B. | 乙炔 | C. | 乙醇 | D. | 乙醛 |
8.关于如图所示的原电池,下列说法正确的是( )
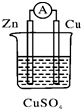

| A. | 电流从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 当有13 g Zn溶解时,外电路中就有0.4 mol电子通过 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
5.下列有关元素或物质性质的说法正确的是( )
| A. | 元素的最高正化合价在数值上一定等于它所在的族序数 | |
| B. | 同周期主族元素的原子半径越小,越难得到电子 | |
| C. | 氟气能从溴化钾溶液中置换出溴单质 | |
| D. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
6.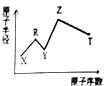 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离子平衡.六种元素的原子半径与原序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 与同主族元素的氢化物相比较,R和Y的氢化物最稳定 | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、Y、Z、T四种元素组成的化合物水溶液一定显碱性 |
7.氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42-、Mg2+、A13+、Fe2+) 经下列流程可制得高纯度硫酸铜晶体如图1:
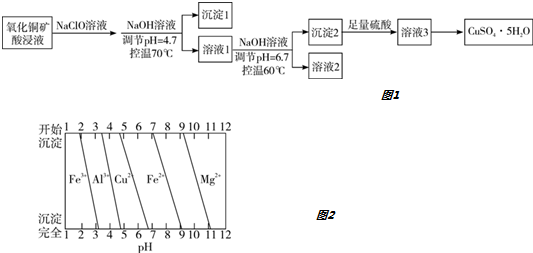
已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )

已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )
| A. | 沉淀1的主要成分为Al(OH)3和Fe(OH)3 | |
| B. | 溶液2中所含金属阳离子只有Mg2+ | |
| C. | 将溶液3蒸干即得CuSO4•5H2O晶体 | |
| D. | 若不加入NaClO溶液,对制得硫酸铜晶体的纯度将无影响 |

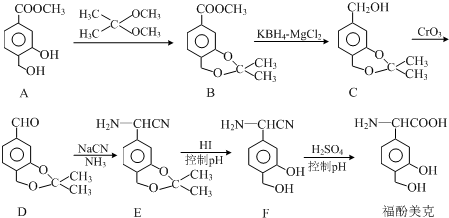
 .
.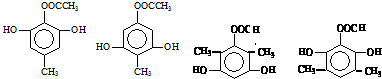 任意一种.
任意一种.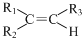 $→_{②Zn/H_{20}}^{①O_{3}}$
$→_{②Zn/H_{20}}^{①O_{3}}$ 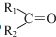 +R3CHO,根据已有知识并结合相关信息,写出以
+R3CHO,根据已有知识并结合相关信息,写出以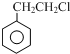 为原料制备
为原料制备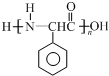 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).