题目内容
8.关于如图所示的原电池,下列说法正确的是( )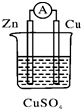
| A. | 电流从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 当有13 g Zn溶解时,外电路中就有0.4 mol电子通过 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
分析 A.电流从正极流向负极;
B.失电子发生氧化反应,得电子发生还原反应;
C.根据锌和转移电子之间的关系式计算;
D.原电池放电时,铜作正极,铜离子得电子发生还原反应在铜极上析出.
解答 解:A.该原电池中较活泼的金属锌作负极,较不活泼的金属铜作正极,电流从Cu电极通过检流计流向Zn电极,故A错误;
B.锌电极上失电子发生氧化反应,Cu电极上得电子发生还原反应,故B错误.
C.铜、锌原电池工作时,若有13g锌被溶解,电路中通过的电子=$\frac{13g}{65g/mol}$×2=0.4mol,故C正确.
D.原电池放电时,铜作正极,铜离子得电子发生还原反应在铜极上析出,电极反应式为Cu2++2e-=Cu,故D错误.
故选C.
点评 本题考查了原电池原理,难度不大,明确原电池中正负极上发生的反应以及电流的流向是解题的关键,注意根据电子与物质之间的关系计算.

练习册系列答案
相关题目
16.借助碱金属和卤族元素的递变性分析下面的推断,其中正确的是( )
| A. | 已知Ca是第4周期、第ⅡA族元素,故Ca(OH)2的碱性比Mg(OH)2的碱性弱 | |
| B. | 已知As是第4周期、第VA族的元素,故AsH3的稳定性比NH3的稳定性强 | |
| C. | 已知Cs的原子半径比Na的原子半径大,故Cs与水反应不如Na与水反应剧烈 | |
| D. | 已知Cl的核电荷数比F的核电荷数大,故Cl的原子半比F的原子半径大 |
13.实验室用100mL 1mol•L-1盐酸与足量锌粉反应制备氢气,下列措施能加快反应速率且不影响产生氢气的量是( )
| A. | 改用100mL2mol•L-1盐酸 | B. | 加入碳酸钠固体 | ||
| C. | 滴加少量CuCl2溶液 | D. | 降低温度 |
20.下列互为同位素的是( )
| A. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、${\;}_{1}^{3}$H2 | B. | ${\;}_{6}^{12}$C、${\;}_{6}^{14}$C | ||
| C. | D2O、H2O | D. | 金刚石、石墨 |
17.下列有关有机化合物的叙述正确的是( )
| A. | 植物油与聚乙烯均能使溴水褪色 | |
| B. | 淀粉与纤维素均为高分子化合物且互为同分异构体 | |
| C. | 蔗糖与麦芽糖的水解产物均为葡萄糖 | |
| D. | 丙烷与2-甲基丙烷的一氯代物均为两种 |
18.室温下,0.1mol下列物质分别与1L0.1mol/LNaOH溶液反应,所得溶液pH最小的是( )
| A. | SO3 | B. | NO2 | C. | Al2O3 | D. | SO2 |

 .
.