题目内容
7.将0.2mol KMnO4在一定温度下加热后生成a mol O2;将剩余固体与过量浓盐酸混合加热又生成b mol Cl2,此时锰元素均以Mn2+形式存在.若a+b=m,则m的值可能为( )| A. | 0.30 | B. | 0.35 | C. | 0.40 | D. | 0.50 |
分析 KMnO4固体在一定温度下加热,反应后的残留固体中与过量的浓盐酸,收集到气体为氯气,根据电子转移守恒,整个过程中,Mn元素获得电子等于O元素、Cl元素获得的电子,则有:0.2×(7-2)=4a+2b,整理得a+b=0.5-a,当高氯酸钾没有分解时,(a+b)达极大值,当高锰酸钾完全分解生成氧气时,生成氧气最多,生成氯气最少,根据方程式计算氧气最大值,进而确定(a+b)的最小值.
解答 解:KMnO4固体在一定温度下加热,反应后的残留固体中与过量的浓盐酸,收集到气体为氯气,根据电子转移守恒,整个过程中,Mn元素获得电子等于O元素、Cl元素获得的电子,则有:0.2×(7-2)=4a+2b,整理得a+b=0.5-a,
当高氯酸钾没有分解时,即a=0,(a+b)达极大值,故(a+b)<0.5,
当高锰酸钾完全分解生成氧气时,生成氧气最多,生成氯气最少,由2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,可知生成氧气最大的物质的量为0.2mol×$\frac{1}{2}$=0.1mol,故a+b≥0.5-0.1=0.4,
故选:C.
点评 本题考查混合物计算、氧化还原反应计算,注意充分利用整个过程中的电子转移守恒解答,关键是用氧气物质的量表示出m的表达式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.某科研小组探究工业废Cu粉(杂质可能含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4•5H2O,实现废物综合利用.他们进行了两组实验,过程如下:
Ⅰ: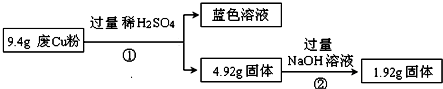
Ⅱ:
(1)废Cu粉中含有的杂质是SiO2、Fe2O3.
(2)分别写出过程①③中发生反应的离子方程式:
①Fe2O3+6H+═2Fe3++3H2O、Al2O3+6H+═2Al3++3H2O、Cu+2Fe3+═2Fe2++Cu2+;③SiO2+2OH-═SiO32-+H2O、Al2O3+2OH-=2AlO2-+H2O.
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(可不必化简).(4)已知25℃时:
从Ⅱ中所得蓝色溶液中分离提纯得到CuSO4•5H2O晶体,需要经过下列步骤:
a、向蓝色溶液中加入一定量的H2O2 溶液;
b、调节溶液的pH为4.0≤pH<5.4之间;
c、然后过滤、结晶,再过滤,可得CuSO4•5H2O.
下列关于实验操作的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH>4的溶液中Fe3+一定不能大量存在.
Ⅰ:

Ⅱ:

(1)废Cu粉中含有的杂质是SiO2、Fe2O3.
(2)分别写出过程①③中发生反应的离子方程式:
①Fe2O3+6H+═2Fe3++3H2O、Al2O3+6H+═2Al3++3H2O、Cu+2Fe3+═2Fe2++Cu2+;③SiO2+2OH-═SiO32-+H2O、Al2O3+2OH-=2AlO2-+H2O.
(3)综合过程Ⅰ、II,计算工业废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(可不必化简).(4)已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
a、向蓝色溶液中加入一定量的H2O2 溶液;
b、调节溶液的pH为4.0≤pH<5.4之间;
c、然后过滤、结晶,再过滤,可得CuSO4•5H2O.
下列关于实验操作的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.上述步骤c中第一次过滤是为了得到滤液,第二次过滤是为了得到固体
D.在pH>4的溶液中Fe3+一定不能大量存在.
12.分子式为C5H10,属于烯烃的同分异构体(包括顺反异构)有( )种.
| A. | 5 | B. | 6 | C. | 7 | D. | 8 |
19.下列对能量转化的认知中,不正确的是( )
| A. | 白炽灯工作时,电能全部转化为光能 | |
| B. | 风力发电时,风能主要转化为电能 | |
| C. | 煤燃烧时,化学能主要转化热能 | |
| D. | 电解水生成H2和O2时,电能主要转化为化学能 |
16.某原子的电子排布式为1s22s22p63s23p63d54s2,下列说法中不正确的是( )
| A. | 该元素原子中共有25个电子 | B. | 该元素原子核外有4个能层 | ||
| C. | 该元素原子最外层共有2个电子 | D. | 该元素原子M电子层共有8个电子 |
17.下列有关物质水解的说法不正确的是( )
| A. | 淀粉、纤维素、蛋白质均属于天然高分子化合物,水解产物都只有一种 | |
| B. | 油脂在碱性条件下水解属于皂化反应,酸性条件下的水解产物为甘油和高级脂肪酸 | |
| C. | 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度 | |
| D. | TiCl4+(x+2)H2O$\stackrel{△}{?}$TiO2•xH2O↓+4HCl 属于水解反应 |
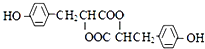
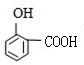 .
.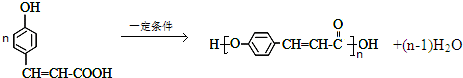 .
. .
.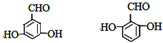 .
.