题目内容
11.亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌.某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究.已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2﹒3H2O,高于38℃时析出晶体的是NaClO2,高于60℃时 NaClO2分解成NaClO3和NaCl.Ba(ClO2)可溶于水.
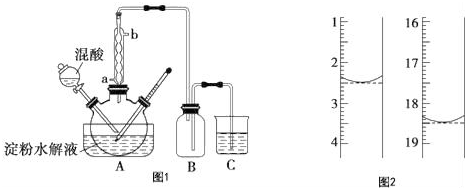
利用如图所示装置进行实验.
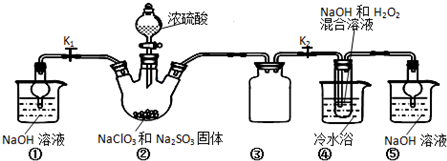
(1)装置①的作用是吸收多余的ClO2气体,防止污染环境,装置③的作用是防止倒吸.
(2)装置②中产生ClO2,涉及反应的化学方程式为2NaClO3+Na2SO3+H2SO4(浓)═2ClO2↑+2Na2SO4+H2O;装置④中反应生成NaClO2的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.
(3)从装置④反应后的溶液获得晶体NaClO2的操作步骤为:①减压,55℃蒸发结晶;②趁热过滤;③用38℃~60℃热水洗涤;④低于60℃干燥,得到成品.如果撤去④中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl.
(4)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作与现象是:取少量晶体溶于蒸馏水,滴加几滴BaCl2溶液,若有白色沉淀出现,则含有Na2SO4,若无白色沉淀出现,则不含Na2SO4.
(5)为了测定NaClO2粗品的纯度,取上述初产品10.0g溶于水配成1L溶液,取出10mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,杂质不参加反应),加入2~3滴淀粉溶液,用0.20mol﹒L-1 Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算NaClO2粗品的纯度90.5%.(提示:2Na2S2O3+I2=Na2S4O6+2NaI)
分析 装置B中制备得到ClO2,所以B中反应为NaClO3和Na2SO3在浓H2SO4的作用生成 ClO2和Na2SO4,二氧化氯和氢氧化钠反应生成NaClO2,B中可能发生Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O,产生的SO2 被带入D中,SO2与H2O2 反应生成硫酸钠,由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl;装置C的作用是安全瓶,有防倒吸作用,从装置D的溶液获得NaClO2晶体,需要蒸发结晶、趁热过滤、洗涤、干燥,装置AE是吸收多余气体防止污染,
(1)本实验产生污染性气体,直接排放会污染环境,故需要尾气处理,装置①就是用碱吸收反应产生的ClO2等尾气;装置③为安全瓶,防止装置②中气体温度降低而产生倒吸;
(2)装置②中产生ClO2,亚硫酸钠具有还原性,在反应中作还原剂,生成硫酸钠,结合原子守恒可知,还有水生成;装置④反应后的溶液获得NaClO2晶体,故装置④中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,然后配平书写方程式;
(3)从溶液中制取晶体,一般采用蒸发结晶、过滤、洗涤、干燥的方法,注意温度控制;由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl;
(4)根据SO42-的检验方法来分析;
(5)根据关系式NaClO2~2I2~4S2O32-进行计算.
解答 解:(1)本实验产生污染性气体,直接排放会污染环境,故需要尾气处理,装置①就是用碱吸收反应产生的ClO2等尾气,当关闭K2时,打开K1,可以吸收反应产生的ClO2气体,防止污染环境,装置③为安全瓶,防止装置②中气体温度降低而产生倒吸,
故答案为:吸收多余的ClO2气体,防止污染环境;防止倒吸;
(2)氯酸钠在酸性溶液中氧化亚硫酸钠为硫酸钠,本身被还原为二氧化氯,反应的化学方程式应为:2NaClO3+Na2SO3+H2SO4(浓)═2ClO2↑+2Na2SO4+H2O,装置④反应后的溶液获得NaClO2晶体,故装置④中生成NaClO2,Cl元素的化合价降低,双氧水应表现还原性,有氧气生成,结合原子守恒可知,还有水生成,配平后方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2,
故答案为:2NaClO3+Na2SO3+H2SO4(浓)═2ClO2↑+2Na2SO4+H2O;2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
(3)为防止析出晶体NaClO2•3H2O,应趁热过滤,由题目信息可知,应控制温度38℃~60℃进行洗涤,低于60℃干燥,如果撤去④中的冷水浴,由题目信息可知,应控制温度38℃~60℃,高于60℃时NaClO2分解成NaClO3和NaCl,所以如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl,
故答案为:用38℃~60℃热水洗涤;NaClO3和NaCl;
(4)SO42-的检验用氯化钡溶液,取少量晶体溶于蒸馏水,然后滴加几滴BaCl2溶液,若有白色沉淀出现,则含有Na2SO4,若无白色沉淀出现,则不含Na2SO4;
故答案为:滴加几滴BaCl2溶液,若有白色沉淀出现,则含有Na2SO4,若无白色沉淀出现,则不含Na2SO4;
(5)令样品中NaClO2的质量分数为a,则:
NaClO2 ~2I2 ~4S2O32-
90.5g 4mol
10.0g×a 0.20mol•L-1×20×10-3L×$\frac{1000ml}{10ml}$,
a=90.5%,
故答案为;90.5%;
点评 本题考查物质的制备、对信息的利用、对装置的理解、氧化还原反应滴定等,理解原理是解题的关键,同时考查学生分析问题、解决问题的能力,题目难度较大,注意氧化还原反应滴定中利用关系式进行的计算.

| A. | CO2的摩尔质量是44g•mol-1,表示1molCO2的质量为44g | |
| B. | 硫酸溶液物质的量的浓度为1mol•L-1表示1L溶液中含有1mol硫酸 | |
| C. | 气体摩尔体积Vm≈22.4mol•L-1,表示1mol任何气体的体积都约为22.4L | |
| D. | 阿伏加德罗常数NA≈6.02×1023mol-1,表示1mol任何粒子集合体所含的粒子数约为6.02×1023 |
| A. | 干冰用作冷冻剂 | B. | 硫酸用于处理碱性废液 | ||
| C. | 氧气用于气焊 | D. | 生石灰用作干燥剂 |
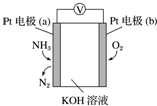 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )| A. | O2在电极b上发生还原反应 | |
| B. | 溶液中OH-向电极a移动 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | 负极的电极反应式为2NH3-6e-+6OH-═N2+6H2O |

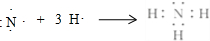 ;
;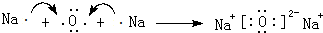 .
.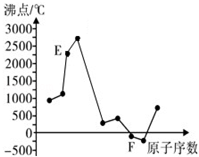 A、B、C、D、E、F是元素周期表中前20号元素,它们的原子序数依次增大.A、B可分别与C组成常见化合物AC、AC2、BC、BC2;D元素的焰色反应呈黄色;E、F两元素单质的沸点与元素原子序数的关系如图(图中原子序数连续).
A、B、C、D、E、F是元素周期表中前20号元素,它们的原子序数依次增大.A、B可分别与C组成常见化合物AC、AC2、BC、BC2;D元素的焰色反应呈黄色;E、F两元素单质的沸点与元素原子序数的关系如图(图中原子序数连续).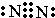 ,化合物AC2的结构式O=C=O;C、D、F对应的简单离子半径由小到大的顺序为Na+<O2-<Cl-(用离子符号表示).
,化合物AC2的结构式O=C=O;C、D、F对应的简单离子半径由小到大的顺序为Na+<O2-<Cl-(用离子符号表示).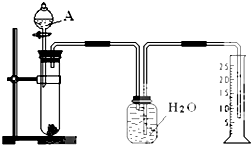 某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数.可供选用的试剂有:浓H2SO4、浓硝酸、6mol•L-1NaOH溶液.请填写下列空白:
某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数.可供选用的试剂有:浓H2SO4、浓硝酸、6mol•L-1NaOH溶液.请填写下列空白: