题目内容
实验室欲配制1mol/L的NaOH溶液90mL,其操作可分为以下各步:
A.用 称取 g NaOH固体,并放在烧杯中用适量蒸馏水溶解,同时用玻璃棒不断搅拌;
B.用约30mL蒸馏水,分成2-3次洗涤 和 ,将每次洗液都转入 里;
C.检查容量瓶口部是否漏水;
D.待烧杯中的NaOH溶液 后才能小心转入容量瓶里;
E.将蒸馏水直接加入容量瓶,至液面接近刻度线 处;
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G.用向容量瓶里逐滴滴入蒸馏水,至液面最低点恰好和刻度线相切.
据此填写:(1)上述各步的空白处.
(2)正确的操作顺序是(填写字母) .
(3)下列是一些同学操作,可能引起实验误差的是(填偏高、偏低、无影响)
A、原容量瓶洗涤后未干燥 B、定容时,俯视刻度线
C、烧杯或玻璃棒未经洗涤 D、称量固体NaOH时已经潮解 .
A.用
B.用约30mL蒸馏水,分成2-3次洗涤
C.检查容量瓶口部是否漏水;
D.待烧杯中的NaOH溶液
E.将蒸馏水直接加入容量瓶,至液面接近刻度线
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G.用向容量瓶里逐滴滴入蒸馏水,至液面最低点恰好和刻度线相切.
据此填写:(1)上述各步的空白处.
(2)正确的操作顺序是(填写字母)
(3)下列是一些同学操作,可能引起实验误差的是(填偏高、偏低、无影响)
A、原容量瓶洗涤后未干燥
C、烧杯或玻璃棒未经洗涤
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据n=cM计算出氢氧化钠的物质的量,再根据m=nM计算出氢氧化钠的质量;烧杯和玻璃棒需要洗涤,洗涤液也要转移到容量瓶中;氢氧化钠溶于水放热,向容量瓶中继续加蒸馏水,至液面接近刻度线1~2cm;
(2)根据配制一定物质的量浓度的溶液的配制步骤进行排序;
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
判断.
(2)根据配制一定物质的量浓度的溶液的配制步骤进行排序;
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
| n |
| V |
解答:
解:(1)称量用托盘天平,没有90ml的容量瓶,应配制100ml,NaOH固体的质量为:1mol/L×0.1L×40g/mol=4.0g;烧杯和玻璃棒需要洗涤,洗涤液也要转移到容量瓶中;氢氧化钠溶于水放热,向容量瓶中继续加蒸馏水,至液面接近刻度线1~2cm,
故答案为:托盘天平;4.0;烧杯;玻璃棒;容量瓶;冷却;1~2cm;
(2)配制100mL 1.00mol?L-1 NaOH溶液的操作步骤有:计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,并用玻璃棒搅拌,加速溶解.冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,正确的操作顺序是:CADBEGF;
(3)A.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
B.定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓度偏高;
C.未洗涤烧杯和玻璃棒,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠的实际质量减小,溶液浓度偏低;
D.NaOH时已经潮解,称取的氢氧化钠偏少,溶液浓度偏低.
故答案为:无影响;偏高;偏低;偏低.
故答案为:托盘天平;4.0;烧杯;玻璃棒;容量瓶;冷却;1~2cm;
(2)配制100mL 1.00mol?L-1 NaOH溶液的操作步骤有:计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,并用玻璃棒搅拌,加速溶解.冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,正确的操作顺序是:CADBEGF;
(3)A.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
B.定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓度偏高;
C.未洗涤烧杯和玻璃棒,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠的实际质量减小,溶液浓度偏低;
D.NaOH时已经潮解,称取的氢氧化钠偏少,溶液浓度偏低.
故答案为:无影响;偏高;偏低;偏低.
点评:本题考查了配制一定物质的量浓度的溶液的方法,难度不大,侧重对学生能力的培养和解题方法的指导和训练,误差分析是本题难点,注意明确分析误差的方法与技巧.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
下列说法中不正确的是( )
| A、物质的量是可以把物质的质量与微观粒子数联系起来的一个基本物理量 |
| B、摩尔是国际单位制中七个基本物理量之一 |
| C、1mol任何微观粒子的质量以克为单位,数值上等于该粒子的相对原子(分子)质量 |
| D、含有6.02×1023个粒子的任何微观粒子集体计量为1摩尔 |
下列实验方案设计正确的是( )
| A、分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 |
| B、失去标签的硝酸银溶液、稀盐酸、氢氧化钠溶液、氯化铝溶液,可以用碳酸铵溶液鉴别 |
| C、将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体 |
| D、检验从火星上带回来的红色物体是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |



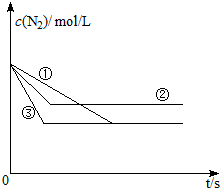 氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
氮化硅是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得: