题目内容
下列叙述正确的是( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O.
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O.
| A、①②③④⑤ | B、①③④⑤ |
| C、①③⑤ | D、②④ |
考点:电解原理,金属的电化学腐蚀与防护
专题:电化学专题
分析:①根据原电池能加速负极金属和电解质的反应速率来回答;
②在原电池中,活泼金属做负极,负极金属更易腐蚀,正极金属被保护;
③根据电镀原理中,镀件和电镀液的选择原则来回答;
④根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼;
⑤铁锈的主要成分为Fe2O3?nH2O.
②在原电池中,活泼金属做负极,负极金属更易腐蚀,正极金属被保护;
③根据电镀原理中,镀件和电镀液的选择原则来回答;
④根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼;
⑤铁锈的主要成分为Fe2O3?nH2O.
解答:
解:①锌跟稀硫酸反应的制取氢气,加入少量硫酸铜溶液后,金属锌可以置换金属铜,形成原电池,原电池能加速负极金属和电解质的反应速率,故①正确;
②白铁(镀锌的铁)中,镀层破损后,Zn为负极,被腐蚀的是Zn,Fe被保护,马口铁(镀锡的铁)中,Fe为负极,被腐蚀的是Fe,Zn被保护,所以镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)铁更耐腐蚀,故②错误;
③根据电镀原理中,镀件作电解槽的阴极,故③正确;
④根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,铝是活泼金属,所以通常采用电解熔融氧化铝的方法冶炼,故④正确;
⑤钢铁吸氧腐蚀生成的铁锈的主要成分为Fe2O3?nH2O,故⑤正确.
故选B.
②白铁(镀锌的铁)中,镀层破损后,Zn为负极,被腐蚀的是Zn,Fe被保护,马口铁(镀锡的铁)中,Fe为负极,被腐蚀的是Fe,Zn被保护,所以镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)铁更耐腐蚀,故②错误;
③根据电镀原理中,镀件作电解槽的阴极,故③正确;
④根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,铝是活泼金属,所以通常采用电解熔融氧化铝的方法冶炼,故④正确;
⑤钢铁吸氧腐蚀生成的铁锈的主要成分为Fe2O3?nH2O,故⑤正确.
故选B.
点评:本题是一道综合知识题目,考查学生对原电池原理的应用知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
下列判断中,正确的是( )
| A、已知25℃时NH4CN显碱性,则25℃时的电离常数K(NH3?H2O)>K(HCN) |
| B、25℃时,Mg(OH)2固体在20 mL0.01 mol?L-1氨水中的Ksp比在20 mL0.01 mol?L-1 NH4Cl溶液中的Ksp小 |
| C、pH试纸测得新制氯水的pH为4 |
| D、FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
标准状况下,将V L氨气溶解在0.1L水中(水的密度近似为1g/ml),所得溶液的密度ρ g/ml,物质浓度为c mol/L,质量分数为ω,则下列关系中不正确的是( )
A、c=
| ||
B、c=
| ||
C、c=
| ||
D、ω=
|
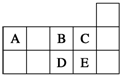 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )| A、D在过量的B中燃烧的主要产物为DB3 |
| B、C的氢化物的水溶液酸性比E的强 |
| C、D与B形成的阴离子可能有DB32-、D2B42- |
| D、E单质中由于形成了氢键,所以很容易液化 |
 用电化学原理研究金属铝具有重要的意义.
用电化学原理研究金属铝具有重要的意义.
