题目内容
 用电化学原理研究金属铝具有重要的意义.
用电化学原理研究金属铝具有重要的意义.(1)已知:Al2O3(s)=Al2O3(溶融1)△H=+28.8kJ?mol-1
Al2O3(熔融1)=2Al(s)+
| 3 |
| 2 |
①工业上利用惰性电极电解熔融的Al2O3冶炼铝,每消耗1000kJ电能时,生成27gAl,则电解过程中能量利用率为
②4Al(s)+3O2(g)=2Al2O3(s)△H=
③利用Al2O3制备无水AlCl3的反应为2Al2O3(s)+6Cl2(g)
| 高温 |
(2)为了防止钢材腐蚀,常采用电解熔融盐法在钢材表面镀铝.熔融盐中铝元素和氯元素仅以AlCl4-、Al2Cl3-形式存在.如图所示:
①钢材表面镀铝时,铝应接电源的
②试分析电镀铝时不用氯化铝水溶液作电解液的原因:
(3)铝一空气-NaOH溶液组成的铝电池性能优越,可用于电动汽车.写出该电池的负极电极反应式
(4)铝可用于处理银器表面的黑斑(Ag2S).将银器置于铝制容器里的食盐水中并与铝接触,形成原电池,可将Ag2S转化为Ag,该过程中食盐水的作用为
考点:电解原理,用盖斯定律进行有关反应热的计算,原电池和电解池的工作原理,化学平衡的影响因素
专题:
分析:(1)①根据Al2O3(熔融1)=2Al(s)+
O2(g)△H=+1600kJ?mol-1,则生成27gAl即1mol时要吸收
=800KJ的热量,据此计算;
②由①Al2O3(s)=Al2O3(溶融1)△H=+28.8kJ?mol-1
②Al2O3(熔融1)=2Al(s)+
O2(g)△H=+1600kJ?mol-1
根据盖斯定律-(①×2+②×2)得,4Al(s)+3O2(g)=2Al2O3(s)据此计算焓变;
③焦炭可消耗产物中的氧气,使c(O2)变小,且燃烧放出热量,温度升高;
(2)①电镀池中镀层金属作阳极,待镀金属作阴极;
②氯化铝溶液中电解氢离子得到电子能力强于铝离子,电解得不到镀铝的结果;
(3)铝一空气-NaOH溶液组成的铝电池中铝做负极失电子,在碱溶液中生成偏铝酸盐;
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,该装置构成原电池,食盐水作电解质溶液,促进溶液的导电性.
| 3 |
| 2 |
| 1600 |
| 2 |
②由①Al2O3(s)=Al2O3(溶融1)△H=+28.8kJ?mol-1
②Al2O3(熔融1)=2Al(s)+
| 3 |
| 2 |
根据盖斯定律-(①×2+②×2)得,4Al(s)+3O2(g)=2Al2O3(s)据此计算焓变;
③焦炭可消耗产物中的氧气,使c(O2)变小,且燃烧放出热量,温度升高;
(2)①电镀池中镀层金属作阳极,待镀金属作阴极;
②氯化铝溶液中电解氢离子得到电子能力强于铝离子,电解得不到镀铝的结果;
(3)铝一空气-NaOH溶液组成的铝电池中铝做负极失电子,在碱溶液中生成偏铝酸盐;
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,该装置构成原电池,食盐水作电解质溶液,促进溶液的导电性.
解答:
解:(1)①由Al2O3(熔融1)=2Al(s)+
O2(g)△H=+1600kJ?mol-1,则生成27gAl即1mol时要吸收
=800KJ的热量,所以电解过程中能量利用率为
×100%=80%,故答案为:80%;
②由①Al2O3(s)=Al2O3(溶融1)△H=+28.8kJ?mol-1
②Al2O3(熔融1)=2Al(s)+
O2(g)△H=+1600kJ?mol-1
根据盖斯定律-(①×2+②×2)得,4Al(s)+3O2(g)=2Al2O3(s)△H=-(28.8×2+1600×2)kJ?mol-1=-3257.6kJ?mol-1;
故答案为:-3257.6;
③焦炭可消耗产物中的氧气,使c(O2)变小;且放出热量,温度升高,导致平衡向正反应方向移动,
故答案为:焦炭可消耗产物中的氧气,使c(O2)变小,且放出热量,温度升高,导致平衡向正反应方向移动;
(2)①电镀池中镀层金属作阳极,待镀金属作阴极,故在钢材表面镀铝,镀铝电解池中,金属铝为阳极,与电源正极相连,故答案为:正;
②在镀铝电解池中电解液采用熔融盐(成分NaCl、KCl,电镀时氯元素和铝元素主要以AlCl4-形式存在).不采用氯化铝溶液的原因是溶液中氢离子得到电子能力强于铝离子,不能实现度铝的目的.
故答案为:氯化铝溶液中,H+得电子能力强于Al3+,电镀池中阴极析出氢气;
(3)铝一空气-NaOH溶液组成的铝电池中铝做负极失电子,在碱溶液中生成偏铝酸盐,反应式为:Al-3e-+4OH-=AlO2-+2H2O;
故答案为:Al-3e-+4OH-=AlO2-+2H2O;
(4)该装置构成原电池,氯化钠溶液作电解质溶液,促进溶液的导电能力,故答案为:作电解质溶液,形成原电池.
| 3 |
| 2 |
| 1600 |
| 2 |
| 800 |
| 1000 |
②由①Al2O3(s)=Al2O3(溶融1)△H=+28.8kJ?mol-1
②Al2O3(熔融1)=2Al(s)+
| 3 |
| 2 |
根据盖斯定律-(①×2+②×2)得,4Al(s)+3O2(g)=2Al2O3(s)△H=-(28.8×2+1600×2)kJ?mol-1=-3257.6kJ?mol-1;
故答案为:-3257.6;
③焦炭可消耗产物中的氧气,使c(O2)变小;且放出热量,温度升高,导致平衡向正反应方向移动,
故答案为:焦炭可消耗产物中的氧气,使c(O2)变小,且放出热量,温度升高,导致平衡向正反应方向移动;
(2)①电镀池中镀层金属作阳极,待镀金属作阴极,故在钢材表面镀铝,镀铝电解池中,金属铝为阳极,与电源正极相连,故答案为:正;
②在镀铝电解池中电解液采用熔融盐(成分NaCl、KCl,电镀时氯元素和铝元素主要以AlCl4-形式存在).不采用氯化铝溶液的原因是溶液中氢离子得到电子能力强于铝离子,不能实现度铝的目的.
故答案为:氯化铝溶液中,H+得电子能力强于Al3+,电镀池中阴极析出氢气;
(3)铝一空气-NaOH溶液组成的铝电池中铝做负极失电子,在碱溶液中生成偏铝酸盐,反应式为:Al-3e-+4OH-=AlO2-+2H2O;
故答案为:Al-3e-+4OH-=AlO2-+2H2O;
(4)该装置构成原电池,氯化钠溶液作电解质溶液,促进溶液的导电能力,故答案为:作电解质溶液,形成原电池.
点评:本题考查了金属的冶炼方法、盖斯定律得应用、化学平衡以及电解原理等知识点,根据电解时离子的放电顺序来分析解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、同周期元素的原子半径以ⅦA族的为最大 |
| B、在周期表中零族元素的单质不全部是气体 |
| C、ⅠA、ⅡA族元素的原子,其半径越大越容易失去电子 |
| D、所有主族元素的原子形成单原子离子时的最高价数都和它的族数相等 |
锂离子电池的应用很广,某种锂离子电池反应原理是:Li1-xCoO2+LiC6
LiCoO2+Li1-xC6下列说法正确的是( )
| 放电 |
| 充电 |
| A、放电过程中,Li向负极区移动 |
| B、正极的电极反应式:LixC6+xe-=xLi+Li1-xC6 |
| C、电子流动方向:负极→外电路→正极→有机电解液→负极 |
| D、充电时阳极电极反应式:LiCoO2-xe-=Li1-xCoO2+x Li |
甲、乙、丙、丁四种物质,在一定条件下能发生如图所示的转化.甲
丙
丁
则符合转化关系的正确组合是( )
| 乙 |
| 乙 |
| 甲 |
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 甲 | Fe | O2 | HNO3 | H2S | NaOH | KOH |
| 乙 | Cl2 | C | Fe | O2 | AlCl3 | SO2 |
| 丙 | FeCl3 | CO2 | Fe(NO2)3 | S | Al(OH)3 | K2SO3 |
| 丁 | FeCl2 | CO | Fe(NO3)2 | SO2 | NaAlO2 | KHSO2 |
| A、只有①②③④ |
| B、只有②③④⑥ |
| C、只有③④⑤⑥ |
| D、只有②③⑤⑥ |
下列叙述正确的是( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O.
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O.
| A、①②③④⑤ | B、①③④⑤ |
| C、①③⑤ | D、②④ |
星际空间存在着以分子形式存在的星际物质.下表为某些星际分子发现年代列表,下列有关说法正确的是( )
( )
| 发现年代 | 1971年 | 1976年 | 1977年 | 1978年 | 1982年 |
| 星际分子 | 氰基乙炔 (HC3N) | 氰基丁二炔 (HC5N) | 氰基已三炔 (HC7N) | 氰基辛四炔 (HC9N) | 氰基癸五炔 (HC11N) |
| A、五种氰基炔互为同素异形体 |
| B、它们都属于烃的衍生物 |
| C、五种氰基互为同系物 |
| D、HC11N属于高分子化合物 |
现有两份等物质的量的某有机物,同温同压下使其分别与过量的Na和足量的NaHCO3反应,分别得到V1 L氢气和V2 L二氧化碳.若V1=V2≠0,则该有机物可能是( )
A、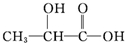 |
| B、HOOC-COOH |
| C、HOCH2CH2OH |
| D、CH3COOH |
 RCOOH+CO2↑②
RCOOH+CO2↑②
