题目内容
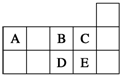 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )| A、D在过量的B中燃烧的主要产物为DB3 |
| B、C的氢化物的水溶液酸性比E的强 |
| C、D与B形成的阴离子可能有DB32-、D2B42- |
| D、E单质中由于形成了氢键,所以很容易液化 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置可知:A为碳元素、B为氧元素、C为氟元素、D为硫元素、E为氯元素,
A.硫在氧气中燃烧生成二氧化硫;
B.氢氟酸是弱酸;
C.碳元素与氧元素可以组成CO32-、C2O42-;
D.氯气分子中不存在氢键.
A.硫在氧气中燃烧生成二氧化硫;
B.氢氟酸是弱酸;
C.碳元素与氧元素可以组成CO32-、C2O42-;
D.氯气分子中不存在氢键.
解答:
解:由元素在周期表中的位置可知:A为碳元素、B为氧元素、C为氟元素、D为硫元素、E为氯元素,
A.硫在氧气中燃烧生成二氧化硫,二氧化硫在催化剂、加热条件下可以转化为三氧化硫,故A错误;
B.氢氟酸是弱酸,盐酸是强酸,盐酸的酸性更强,故B错误;
C.碳元素与氧元素可以组成CO32-、C2O42-,故C正确;
D.氯气分子中不存在氢键,故D错误;
故选C.
A.硫在氧气中燃烧生成二氧化硫,二氧化硫在催化剂、加热条件下可以转化为三氧化硫,故A错误;
B.氢氟酸是弱酸,盐酸是强酸,盐酸的酸性更强,故B错误;
C.碳元素与氧元素可以组成CO32-、C2O42-,故C正确;
D.氯气分子中不存在氢键,故D错误;
故选C.
点评:本题考查位置结构性质关系、元素化合物性质等,为高频考点,侧重于学生的分析能力的考查,难度不大,注意整体把握元素周期表、全面掌握基础知识,C为易错点,容易忽略草酸根.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述正确的是( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O.
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O.
| A、①②③④⑤ | B、①③④⑤ |
| C、①③⑤ | D、②④ |
现有两份等物质的量的某有机物,同温同压下使其分别与过量的Na和足量的NaHCO3反应,分别得到V1 L氢气和V2 L二氧化碳.若V1=V2≠0,则该有机物可能是( )
A、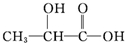 |
| B、HOOC-COOH |
| C、HOCH2CH2OH |
| D、CH3COOH |
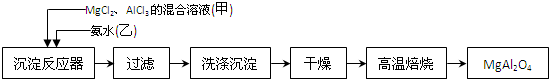
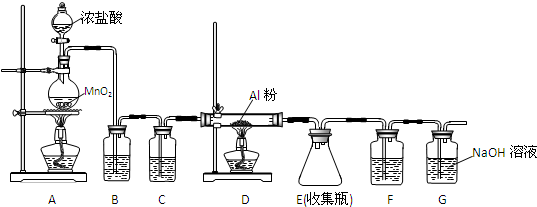

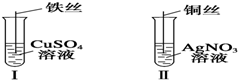 按如图所示操作,充分反应后:
按如图所示操作,充分反应后: