题目内容
4.在烃的分子中去掉2个氢原子形成一个双键是吸热反应,大约需要117kJ/mol~125kJ/mol的热量,但1,3-环己二烯失去2个氢原子变成苯是放热反应,反应热为23.4kJ/mol.以上事实表明( )| A. | 1,3-环己二烯加氢是吸热反应 | |
| B. | 完全燃烧时1,3-环己二烯比苯放热多 | |
| C. | 苯加氢生成环己烷是吸热反应 | |
| D. | 苯比1,3-环己二烯稳定 |
分析 旧键的断裂需要吸收能量,新键的生成需要释放能量,当反应物的能量高于生成物的能量.则为放热反应,反之为吸热反应,物质具有的能量越低越稳定,结合题目信息来回答.
解答 解:A.在烃的分子中去掉2个氢原子形成一个双键是吸热反应,则1,3-环己二烯加氢是放热反应,故A错误;
B.没有告诉1,3-环己二烯与苯的物质的量关系,无法确定放热多少,故B错误;
C.通过题中信息无法确定,苯加氢生成环己烷是吸热反应还是放热反应,故C错误;
D.1,3-环己二烯失去两个氢原子变成苯是放热反应,说明1,3-环己二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故D正确.
故选D.
点评 本题考查了化学反应中的能量变化、物质具有的能量与稳定性的关系,题目难度中等,侧重于考查学生的分析能力和对题中信息的应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列物质分类或归类正确的一组是( )
| A. | 液氨、液氯、干冰、碘化银均为化合物 | |
| B. | 明矾、小苏打、醋酸、次氯酸均为电解质 | |
| C. | 碘酒、牛奶、豆浆、漂白粉均为胶体 | |
| D. | Na2O2、Na2CO3、Na2SiO3、KNO3均为盐 |
15.物质的量浓度相同时,下列既能跟NaOH溶液反应又能跟盐酸反应的溶液中,pH最小的是( )
| A. | Na2SO3溶液 | B. | NH4HCO3溶液 | C. | NaHCO3溶液 | D. | NaHSO3溶液 |
19.短周期元素X、Y、Z、W的原子序数依次增大,它们分别位于不同的主族,X的最高正价与最低负价代数和为0,Y为金属元素,Y与Z最外层电子数之和与W最外层电子数相等,X与W所在族序数之和等于10.下列说法正确的是( )
| A. | 简单氢化物的热稳定性:Z>W | B. | 最高价氧化物的水化物的酸性:X<Z | ||
| C. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | D. | 沸点:XW2>Y2W |
9.下列关于化学平衡常数的说法中错误的是( )
| A. | 某特定反应的平衡常数只与温度有关 | |
| B. | 催化剂不能改变平衡常数的大小 | |
| C. | 平衡常数发生改变,化学平衡必发生改变 | |
| D. | 化学平衡移动时,平衡常数必改变 |
13.下列有关说法正确的是( )
| A. | 常温下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | pH=3的醋酸溶液中:c(H+)=c(CH3COO-)=3.0mol•L-1 | |
| C. | 某溶液中由水电离出的c(OH-)=1×10-amol•L-1,若a>7时,则该溶液的pH可能为a | |
| D. | 常温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+ )>c(H+)>c(OH-) |
14.洗涤下列仪器时,选用的试剂(括号中的物质)不正确的是( )
| A. | 做过木炭还原氧化铜实验的硬质玻璃管(盐酸) | |
| B. | 长期存放氯化铁溶液的试剂瓶(稀硫酸) | |
| C. | 做过碘升华实验的试管(酒精) | |
| D. | 沾有油污的烧杯(纯碱溶液) |
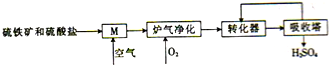 煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示.
煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示.