题目内容
12.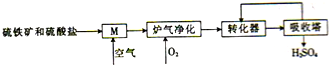 煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示.
煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示.回答下列问题:
(1)硫铁矿和硫酸盐燃烧的装置M的名称为沸腾炉.
(2)炉气净化过程包括除尘(防止堵塞管道)、洗涤(除去有害物质,防止在转化器中使催化剂中毒)和干燥,干燥的目的是防止硫的氧化物与水反应生成酸雨腐蚀设备.
(3)转化器中的催化剂是V2O3,而反应条件选择400~500℃和常压的原因是400~500℃时催化剂的活性最大,常压下二氧化硫的转化率已经很高,再增加压强,会提高设备成本.已知每生成1molSO2(g),释放148.5kJ热量,写出该反应的热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-297kJ/mol,该反应过程中通入稍过量O2的目的是提高二氧化硫的转化率.
(4)实验生产中常采用两次转化,其目的是提高原料利用率,流程中可循环利用的物质是SO2和O2.
(5)该方法合成硫酸的优点是变废为宝,减少环境污染;按目前技术水平生产硫酸的流程中,反应热的利用约为$\frac{3}{5}$,试提出利用富余反应热的方法:利用余热发电.
分析 硫铁矿和硫酸盐燃烧生成二氧化硫,二氧化硫与氧气在转化器中反应生成三氧化硫,三氧化硫吸收生成硫酸.
(1)硫铁矿和硫酸盐在沸腾炉中燃烧;
(2)硫的氧化物与水反应生成酸性物质;
(3)400~500℃时催化剂的活性最大,常压下二氧化硫的转化率已经很高;每生成1molSO2(g),释放148.5kJ热量,每生成2molSO2(g),释放297kJ热量,增大一种反应物的量可提高另一种反应物的转化率;
(4)两次转化可提高原料利用率,SO2和O2可循环利用;
(5)废气中的二氧化硫变废为宝,减少环境污染.
解答 解:(1)硫铁矿和硫酸盐在沸腾炉中燃烧,故答案为:沸腾炉;
(2)硫的氧化物与水反应生成酸性物质,腐蚀设备,故答案为:防止硫的氧化物与水反应生成酸雨腐蚀设备;
(3)400~500℃时催化剂的活性最大,常压下二氧化硫的转化率已经很高,再增加压强,会提高设备成本;每生成1molSO2(g),释放148.5kJ热量,每生成2molSO2(g),释放297kJ热量,2SO2(g)+O2(g)?2SO3(g)△H=-297kJ/mol;增大一种反应物的量可提高另一种反应物的转化率,提高二氧化硫的转化率,故答案为:400~500℃时催化剂的活性最大,常压下二氧化硫的转化率已经很高,再增加压强,会提高设备成本;2SO2(g)+O2(g)?2SO3(g)△H=-297kJ/mol;提高二氧化硫的转化率;
(4)两次转化可提高原料利用率,SO2和O2可循环利用,故答案为:提高原料利用率;SO2和O2;
(5)废气中的二氧化硫变废为宝,减少环境污染,可利用余热发电或取暖,故答案为:变废为宝,减少环境污染;利用余热发电.
点评 本题考查环境污染及治理,为高频考点,侧重于化学与生活、生产、能源与环境的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.

| A. | H+、I-、NO3-、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | K+、Cu2+、SO42-、NO3- | D. | NH4+、OH-、Cl-、HCO3- |
| A. | 采用催化转化技术,可将汽车尾气中的一氧化碳和氮氧化物转化为无毒气体 | |
| B. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| C. | 利用风能、太阳能等清洁能源代替化石燃料,可减少环境污染 | |
| D. | 氮化硅陶瓷是一种新型无机非金属材料 |
| A. | 1,3-环己二烯加氢是吸热反应 | |
| B. | 完全燃烧时1,3-环己二烯比苯放热多 | |
| C. | 苯加氢生成环己烷是吸热反应 | |
| D. | 苯比1,3-环己二烯稳定 |
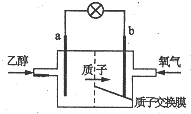 新型乙醇燃料电池比甲醇燃料电池的效率高出32倍,且更安全.其结构如图所示,它用碘酸类质子溶剂,在200℃左右时供电,已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是( )
新型乙醇燃料电池比甲醇燃料电池的效率高出32倍,且更安全.其结构如图所示,它用碘酸类质子溶剂,在200℃左右时供电,已知电池总反应式为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是( )| A. | 电池工作时电流由b极沿导线经灯泡到a极 | |
| B. | a极为电池的负极,该电极发生氧化反应 | |
| C. | 电池正极的电极反应式为O2+2H2O+4e-=4OH- | |
| D. | 电池工作时,23g乙醇被氧化转移电子式为6mol |
| A. | 第2min时,c(Fe2+)=0.01 mol•L-1 | |
| B. | 混合溶液中,c(K+)=0.01 mol•L-1 | |
| C. | 0~2min内,v(I-)=0.01 mol•L-1•min-1 | |
| D. | 第2min时,c(Fe3+)=0.01 mol•L-1 |