题目内容
15.物质的量浓度相同时,下列既能跟NaOH溶液反应又能跟盐酸反应的溶液中,pH最小的是( )| A. | Na2SO3溶液 | B. | NH4HCO3溶液 | C. | NaHCO3溶液 | D. | NaHSO3溶液 |
分析 四种溶液中,既能与NaOH溶液反应,又能与盐酸反应的是NH4HCO3溶液、NaHSO3溶液和NaHCO3溶液,其中NH4HCO3是弱酸弱碱盐,发生双水解,由于氨水的碱性强于碳酸的酸性,故溶液显碱性;亚硫酸氢根离子电离大于水解,溶液显酸性,碳酸氢根离子电离小于水解,显碱性;据此解答
解答 解:四种溶液中,既能与NaOH溶液反应,又能与盐酸反应的是NH4HCO3溶液、NaHSO3溶液和NaHCO3溶液.
其中NH4HCO3是弱酸弱碱盐,发生双水解,由于CH3COONH4溶液显中性,可知CH3COOH的酸性等于氨水的碱性,而碳酸的酸性弱于CH3COOH,故氨水的碱性强于碳酸的酸性,故NH4HCO3溶液显碱性;
碳酸氢根离子电离小于水解,故NaHCO3溶液显碱性;
亚硫酸氢根离子电离大于水解,故NaHSO3溶液显酸性.
故选D.
点评 本题考查了元素化合物知识,熟悉常见既能与酸反应又能与碱反应的物质,熟悉盐类电离、水解规律是解题关键,题目难度中等.

练习册系列答案
相关题目
6.下列各组离子能大量共存的是( )
| A. | K+、Fe3+、Cl-、SCN- | B. | NH4+、H+、NO3-、SO42- | ||
| C. | Ba2+、Na+、HCO3-、SO42- | D. | Fe2+、K+、MnO4-、OH- |
20.能在水溶液中大量共存的一组离子是( )
| A. | H+、I-、NO3-、SiO32- | B. | Ag+、Fe3+、Cl-、SO42- | ||
| C. | K+、Cu2+、SO42-、NO3- | D. | NH4+、OH-、Cl-、HCO3- |
7.化学与生活、能源、环境等密切相关.下列描述错误的是( )
| A. | 采用催化转化技术,可将汽车尾气中的一氧化碳和氮氧化物转化为无毒气体 | |
| B. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮的氧化物无关 | |
| C. | 利用风能、太阳能等清洁能源代替化石燃料,可减少环境污染 | |
| D. | 氮化硅陶瓷是一种新型无机非金属材料 |
4.在烃的分子中去掉2个氢原子形成一个双键是吸热反应,大约需要117kJ/mol~125kJ/mol的热量,但1,3-环己二烯失去2个氢原子变成苯是放热反应,反应热为23.4kJ/mol.以上事实表明( )
| A. | 1,3-环己二烯加氢是吸热反应 | |
| B. | 完全燃烧时1,3-环己二烯比苯放热多 | |
| C. | 苯加氢生成环己烷是吸热反应 | |
| D. | 苯比1,3-环己二烯稳定 |
5.某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
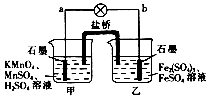

| A. | b电极上发生还原反应 | |
| B. | 甲烧杯中溶液的pH逐渐减小 | |
| C. | 电池工作时,盐桥中的SO42-移向甲烧杯 | |
| D. | 外电路的电流方向是从a到b |