题目内容
12. 化学反应原理在科研和生产中有广泛应用.
化学反应原理在科研和生产中有广泛应用.(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:TaS2(s)+2I2(g)?TaI4(g)+S2(g):△H>0 ( I)反应( I)的平衡常数表达式K=$\frac{c(TaI{\;}_{4})c(S{\;}_{2})}{c{\;}^{2}({I}_{2})}$;若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为66.7%.
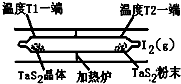
(2)如图所示,反应( I)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量
I2(g),一段时间后,在温度为T1的一端得到了纯净的TaS2晶体,则温度T1<T2(选填“>”、
“<”或“=”).上述反应体系中循环使用的物质是I2.
(3)利用I2的氧化性可测定钢铁中硫的含量.做法是将钢铁中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为淀粉溶液,滴定反应的离子方程式为:H2SO3+I2+H2O=4H++SO42-+2I-.
(4)25℃时,H2SO3?HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=1.0×10-12mol/L,若向NaHSO3溶液中加入少量的I2,则溶液中$\frac{c({H}_{3}S{O}_{3})}{c(HS{O}_{3}^{-})}$将增大(填“增大”“减小”或“不变”).
分析 (1)通过题意求出平衡浓度,带入K值可以得出转化率为66.7%;
(2)通过题意温度T2端利于反应正向进行,为高温,温度T1端利于反应向左进行,为低温,所以T1<T2;
(3)因为I2遇到淀粉会变蓝色,所以可以用淀粉溶液作指示剂;
(4)根据Ka=$\frac{[HS{{O}_{3}}^{-}]•[H+]}{[{H}_{2}SO{\;}_{3}]}$,Kh=$\frac{[H{\;}_{2}SO{\;}_{3}]•K{\;}_{W}}{[HS{O}_{3}{\;}^{-}]•[H{\;}^{+}]}$,代入数据进行计算.
解答 解:(1)根据题意反应(Ⅰ)的平衡常数表达式K=$\frac{c(TaI{\;}_{4})c(S{\;}_{2})}{c{\;}^{2}({I}_{2})}$;
若K=1,设 I2的平衡转化率为x,则参加反应的为xmol,平衡时生成TaI4和S2各0.5xmol,剩余I2为(1-x)mol,
根据K=$\frac{c(TaI{\;}_{4})c(S{\;}_{2})}{c{\;}^{2}({I}_{2})}$=$\frac{0.5x×0.5x}{(1-x){\;}^{2}}$=1,
解之得:x=66.7%,
故答案为:$\frac{c(TaI{\;}_{4})c(S{\;}_{2})}{c{\;}^{2}({I}_{2})}$;66.7%;
(2)由所给方程式可知该反应为吸热反应,通过题意温度T2端利于反应正向进行,为高温,温度T1端利于反应向左进行,为低温,所以T1<T2,I2是可以循环使用的物质;
故答案为:<;I2;
(3)因为I2遇到淀粉会变蓝色,所以可以用淀粉溶液作指示剂.离子反应:H2SO3+I2+H2O=4H++SO42-+2I-,
故答案为:淀粉溶液;H2SO3+I2+H2O=4H++SO42-+2I-;
(4)Ka=$\frac{[HS{{O}_{3}}^{-}]•[H+]}{[{H}_{2}SO{\;}_{3}]}$,HSO3-+H2O?H2SO3+OH-,Kh=$\frac{[H{\;}_{2}SO{\;}_{3}]•K{\;}_{W}}{[HS{O}_{3}{\;}^{-}]•[H{\;}^{+}]}$=1.0×102×1.0×10-14=1.0×10-12,当加入少量I2时,碘把弱酸(亚硫酸)氧化成强酸(硫酸、氢碘酸),溶液酸性增强,[H+]增大,但是温度不变,Kh不变,则 $\frac{c(H{\;}_{2}S{O}_{3})}{c(HSO{\;}_{3}{\;}^{-})}$增大,
故答案为:1.0×10-12;增大.
点评 本题考查化学平衡常数的表达式及其计算,平衡转化率等知识,为高考常见题型,难度较大,侧重分析问题的能力的考查,注意平衡相关知识的灵活运用.

| A. | 5min内用O2表示的反应速率为0.12mol/(L•min) | |
| B. | 加入催化剂,可使该反应的化学反应速率加快,△H变小 | |
| C. | SO2的平衡浓度为0.12mol/L | |
| D. | 达到平衡时,若增大容器的体积,则该反应的化学反应速率减慢 |
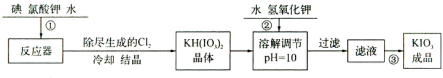
(1)已知步骤①反应器发生的反应为:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑,
该反应的还原产物为KCl、Cl2;
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,你建议的方法是降温结晶.
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
(3)①已知:
测定加碘食盐中碘的含量,学生甲设计的实验步骤如下:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.00×10-3mol•L-1的Na2S2O3溶液10.0mL,恰好反应完全.则加碘食盐样品中的碘元素含量是$\frac{1270}{3w}$mg•kg-1(以含w的代数式表示).
②学生乙又进行了下列实验:
| 操作步骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液 | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL0.1mol•L-1KI溶液,振荡 | 溶液无变化 |
| 然后再滴入1mol•L-1的H2SO4,充分振荡 | 溶液变蓝色 |
根据学生乙的实验结果,请对学生甲的实验结果作出简要评价:偏大,过量的I-会被空气中的O2氧化为I2 .
(4)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①根据上述实验现象,加碘盐中可能含有的物质中不能确定的是Mg2+.
②第二份试液中加入足量KI固体后,反应的离子方程式为2Fe3++2I-=2Fe2++I2、IO3-+5I-+6H+═3I2+3H2O.
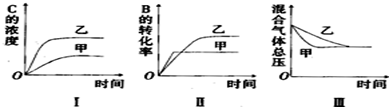
下列判断正确的是( )
| A. | 图I研究的可能是不同催化剂对反应的影响,且乙使用的催化剂效率较高 | |
| B. | 图Ⅱ研究的可能是压强对反应的影响,且甲的压强较高 | |
| C. | 图Ⅱ研究的可能是温度对反应的影响,且甲的温度较高 | |
| D. | 图Ⅲ研究的可能是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| A. | 漂白粉在溶液中存在平衡:ClO-+H2O?HClO+OH-,加少量NaOH能提高其漂白效率 | |
| B. | 硫酸钡难溶子水,但硫酸钡属于强电解质 | |
| C. | 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏大 | |
| D. | 物质的量浓度相同的四种溶液:①氯化铵②硫酸氢铵 ③次氯酸铵④碳酸铵的pH:④>②>①>③ |
| A. | 1 mol | B. | 0.5 mol | C. | 0.75 mol | D. | 0.25 mol |
| A. | 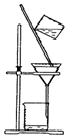 | B. |  | ||
| C. |  | D. |  |
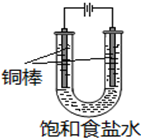 CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.
CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.