题目内容
10.设NA表示阿伏加德罗常数.下列说法正确的是( )| A. | 标准状况下,11.2L N2O4中含有的分子数目为0.5NA | |
| B. | 常温常压下,10.4g苯乙烯中含有的碳碳双键数目为0.1NA | |
| C. | 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | |
| D. | 常温常压下,0.1mol单质硅和二氧化硅中含有的共价键数目都是0.2NA |
分析 A.N2O4的熔点-11.23℃,沸点21.5℃;
B.苯分子中不含碳碳双键;
C.氯气与水反应生成氯化氢和次氯酸,反应为可逆反应;
D.1mol 晶体硅中含有2molSi-Si共价键;1mol二氧化硅中含有的共价键4mol.
解答 解:A.标况下四氧化二氮为液体,不能使用气体摩尔体积,故A错误;
B.10.4g苯乙烯物质的量为0.1mol,含有的碳碳双键数目为0.1NA,故B正确;
C.标准状况下,0.1mol Cl2溶于水,氯气与水反应为可逆反应,不能进行到底,所以转移的电子数目小于0.1NA,故C错误;
D.常温常压下,0.1mol单质硅含有的共价键数目是0.2NA,0.1mol二氧化硅中含有的共价键数目是0.4NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,主要苯乙烯、二氧化硅的结构,题目难度不大.

练习册系列答案
相关题目
20.假酒引起中毒的主要成分是( )
| A. | 甲醇 | B. | 乙醇 | C. | 甲醛 | D. | 乙酸乙酯 |
5.下列说法正确的是( )
| A. | 盐酸的导电能力一定大于醋酸 | |
| B. | 在氨水中加入无水醋酸,溶液的导电能力基本不变 | |
| C. | 在氢氧化钡的稀溶液中,c(OH-)=2c(Ba2+) | |
| D. | 在磷酸的稀溶液中,c(H+)=3c(PO43-) |
15.下列实验装置、操作能达到实验目的是( )
| A. | 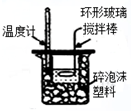 测定中和热 | B. | 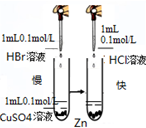 反应快慢 | C. | 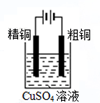 粗铜的电解精炼 | D. | 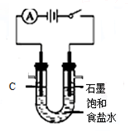 电解食盐水 |
2.下列卤代烃在KOH醇溶液中加热不反应的是( )
①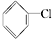 ②
②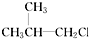 ③(CH3)3CCH2Cl ④CHCl2CHBr2⑤
③(CH3)3CCH2Cl ④CHCl2CHBr2⑤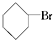 ⑥CH3Cl.
⑥CH3Cl.
①
 ②
②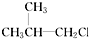 ③(CH3)3CCH2Cl ④CHCl2CHBr2⑤
③(CH3)3CCH2Cl ④CHCl2CHBr2⑤ ⑥CH3Cl.
⑥CH3Cl.| A. | 全部 | B. | ②③⑤ | C. | ①③⑥ | D. | ②④ |
8.下列关于锂的说法正确的是( )
| A. | 碱金属中Li的还原性最强 | B. | 碱金属阳离子,氧化性最强的是Li+ | ||
| C. | 和Li同一主族的都是金属元素 | D. | Li在空气中加热生成过氧化锂 |
9.下列元素的原子在形成不同的物质中,既能形成离子键,又能形成极性键和非极性键的是( )
| A. | K | B. | Ca | C. | I | D. | Ne |
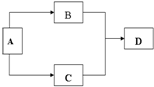 由主族元素组成的A、B、C、D四种常见物质,有如图所示转换关系(部分反应物、生成物没有列出).且四种物质均含有同一种元素.
由主族元素组成的A、B、C、D四种常见物质,有如图所示转换关系(部分反应物、生成物没有列出).且四种物质均含有同一种元素.