题目内容
1.下列关于化学键的说法正确的是( )①含有金属元素的化合物一定是离子化合物
②第ⅠA族和第ⅦA族原子化合时,一定生成离子键
③由非金属元素形成的化合物一定不是离子化合物
④活泼金属与非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物
⑥离子化合物中可能同时含有离子键和共价键
⑦非极性键只存在于双原子单质分子中
⑧不同元素组成的多原子分子中的化学键一定都为极性键.
| A. | ①②⑤ | B. | ④⑤⑥ | C. | ①③④ | D. | ②③⑤ |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含有离子键的化合物为离子化合物,只含共价键的化合物是共价化合物,离子化合物中可能含有共价键,以此来解答.
解答 解:①含有金属元素的化合物不一定是离子化合物,如氯化铝为共价化合物,故错误;
②第ⅠA族和第ⅦA族原子化合时,不一定生成离子键,如H与卤素原子形成共价键,故错误;
③由非金属元素形成的化合物可能为离子化合物,如铵盐,故错误;
④活泼金属与非金属化合时,能形成离子键,如Na、K分别与F、Cl等形成离子键,故正确;
⑤含有离子键的化合物一定是离子化合物,故正确;
⑥离子化合物中可能同时含有离子键和共价键,如NaOH中含离子键和共价键,故正确;
⑦非极性键不仅存在于双原子单质分子中,还可存在化合物转化,如过氧化氢、过氧化钠中均存在,故错误;
⑧不同元素组成的多原子分子中的化学键不一定都为极性键,如过氧化氢中含H-O极性键和O-O非极性键,故错误;
故选B.
点评 本题考查化学键及化合物的类型,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键及实例分析,题目难度不大.

练习册系列答案
相关题目
9.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍.则下列有关说法中正确的是( )
| A. | X的氢化物溶于水显酸性 | |
| B. | Z的氧化物的水化物一定是强酸 | |
| C. | Y的氧化物是离子化合物 | |
| D. | X和Z的最高价氧化物对应的水化物都是弱酸 |
13.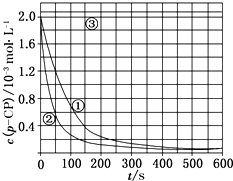 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比实验.
(1)请完成以下实验设计表中横线上的内容.
[数据处理]实验测得p-CP的浓度随时间变化的关系如图.
(2)根据如图实验①曲线,计算降解反应50~150s内的反应速率:v(p-CP)=8.0×10-6mol•L-1•s-1. (3)实验①、②表明温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:H2O2在温度过高时迅速分解.
(4)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来.根据上图中的信息,给出一种迅速停止反应的方法:在溶液中加入碱溶液,使溶液的pH大于或等于10.
 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比实验.
(1)请完成以下实验设计表中横线上的内容.
| 实验编号 | 实验目的 | T/K | pH | c/10-3 mol•L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | 313 | |||
| ③ | 探究溶液的pH对降解反应速率的影响 | 298 | 10 | 6.0 | 0.30 |
(2)根据如图实验①曲线,计算降解反应50~150s内的反应速率:v(p-CP)=8.0×10-6mol•L-1•s-1. (3)实验①、②表明温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:H2O2在温度过高时迅速分解.
(4)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来.根据上图中的信息,给出一种迅速停止反应的方法:在溶液中加入碱溶液,使溶液的pH大于或等于10.
10.设NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 标准状况下,11.2L N2O4中含有的分子数目为0.5NA | |
| B. | 常温常压下,10.4g苯乙烯中含有的碳碳双键数目为0.1NA | |
| C. | 标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA | |
| D. | 常温常压下,0.1mol单质硅和二氧化硅中含有的共价键数目都是0.2NA |
 .
.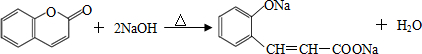 .
. (任意2种)(任写两种).
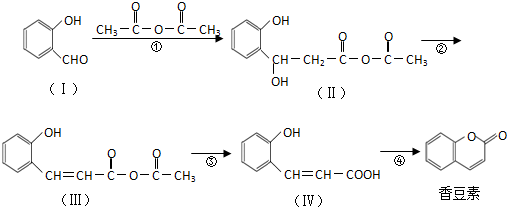
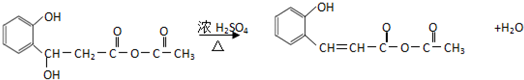
(任意2种)(任写两种).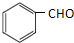 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为 .
.