题目内容
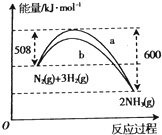 如图,a曲线是298K101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
如图,a曲线是298K101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 KJ/mol |
| B、b曲线是升高温度时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热减少 |
| D、在298K体积一定的条件下,通入1molN2和3molH2反应后放出的热量为Q1KJ,若通入2molN2和6molH2反应后放出的热量为Q2KJ,则184>Q2>2Q1 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、从热化学方程式的要求分析;
B、从催化剂的作用分析;
C、从催化剂的效果分析;
D、从化学平衡的移动与反应热的具体数值分析.
B、从催化剂的作用分析;
C、从催化剂的效果分析;
D、从化学平衡的移动与反应热的具体数值分析.
解答:
解:A、热化学方程式必须注明物质的状态,故A错误.
B、b曲线的活化能降低,是加入催化剂的原因,故B错误;
C、催化剂降低活化能,不改变反应热数值,故C错误;
D、通入2molN2和6molH2后,体积一定,压强增大,反应向正反应方向移动,故Q2>2Q1,又因为反应为可逆反应,不会反应完全,故184>Q2,故D准确;
故选D.
B、b曲线的活化能降低,是加入催化剂的原因,故B错误;
C、催化剂降低活化能,不改变反应热数值,故C错误;
D、通入2molN2和6molH2后,体积一定,压强增大,反应向正反应方向移动,故Q2>2Q1,又因为反应为可逆反应,不会反应完全,故184>Q2,故D准确;
故选D.
点评:本题考查化学能与热能的相互转化,注意加入催化剂能降低活化能,不改变反应热,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
对于复分解反应:X+Y=Z+W,下列叙述正确的( )
| A、若Z是强酸,则X或Y必有一种是酸 |
| B、若Y是强碱,X是盐,则Z或W必有一种是弱碱 |
| C、若W是弱碱,Z是盐,则X或Y必有一种是强碱 |
| D、若X是强酸,Y是盐,反应后可能有强酸或弱酸生成 |
NA代表阿伏伽德罗常数值,下列说法正确的是( )
| A、在1L0.1mol/L Na2SO3溶液中,离子总数小于0.3NA |
| B、向FeI2溶液中通入氯气,当有2molFe2+被氧化,转移电子的数目为2NA |
| C、常温常压下,46g液态N2O4中含有的分子数为0.5NA |
| D、1mol Na2O和Na2O2混合物中含有阴、阳离子总数是NA |
下列说法正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、任何放热反应在常温条件下一定能够发生 |
| C、反应物和生成物所具有的总能量的差决定了化学反应是放热还是吸热 |
| D、构成物质微粒间的化学键键能越小,该物质的能量就越低,物质越稳定 |
下列变化需克服相同类型作用力的是( )
| A、碘和干冰的升华 |
| B、硅和C60的熔化 |
| C、溴和汞的气化 |
| D、二氧化硅和铁分别受热熔化 |
已知m1g气体A与m2g气体B所含的分子数相等,下列说法中正确的是( )
A、1个A分子的质量是1个B分子的质量的
| ||
B、同温同体积等质量的A与B的压强之比为
| ||
C、同温同质量的A与B的分子数之比为
| ||
D、同温同压下A与B的密度之比为
|
一定条件下存在反应:H2(g)+I2(g)?2HI(g)△H<0,现有三个相同的1L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol H2和1mol I2(g),在Ⅱ中充入2molHI(g),在Ⅲ中充入2mol H2和2mol I2(g),700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深 |
| D、容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1 |