题目内容
已知m1g气体A与m2g气体B所含的分子数相等,下列说法中正确的是( )
A、1个A分子的质量是1个B分子的质量的
| ||
B、同温同体积等质量的A与B的压强之比为
| ||
C、同温同质量的A与B的分子数之比为
| ||
D、同温同压下A与B的密度之比为
|
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:m1g气体A与m2g气体B所含的分子数相等,说明二者的物质的量相等,则A、B的摩尔质量之比为m1:m2,
A.每个分子的质量等于气体质量除以气体分子个数;
B.同温同体积等质量时,压强之比等于摩尔质量的反比;
C.同温同质量时,分子个数之比等于其摩尔质量的反比;
D.同温同压下,气体摩尔体积相等,密度之比等于其摩尔质量之比.
A.每个分子的质量等于气体质量除以气体分子个数;
B.同温同体积等质量时,压强之比等于摩尔质量的反比;
C.同温同质量时,分子个数之比等于其摩尔质量的反比;
D.同温同压下,气体摩尔体积相等,密度之比等于其摩尔质量之比.
解答:
解:m1g气体A与m2g气体B所含的分子数相等,说明二者的物质的量相等,则A、B的摩尔质量之比为m1:m2,
A.每个分子的质量等于气体质量除以气体分子个数,所以1个A分子的质量是1个B分子的质量的
倍,故A正确;
B.同温同体积等质量时,压强之比等于摩尔质量的反比,所以其压强之比为m2:m1,故B错误;
C.同温同质量时,分子个数之比等于其摩尔质量的反比,所以其分子个数之比为m2:m1,故C错误;
D.同温同压下,气体摩尔体积相等,密度之比等于其摩尔质量之比,所以密度之比为m1:m2,故D错误;
故选A.
A.每个分子的质量等于气体质量除以气体分子个数,所以1个A分子的质量是1个B分子的质量的
| m1 |
| m2 |
B.同温同体积等质量时,压强之比等于摩尔质量的反比,所以其压强之比为m2:m1,故B错误;
C.同温同质量时,分子个数之比等于其摩尔质量的反比,所以其分子个数之比为m2:m1,故C错误;
D.同温同压下,气体摩尔体积相等,密度之比等于其摩尔质量之比,所以密度之比为m1:m2,故D错误;
故选A.
点评:本题考查阿伏伽德罗定律及其推论,明确物质的量公式中各个物理量的关系是解本题关键,注意前提条件限制,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组物质的性质比较中,正确的是( )
| A、酸性:HClO4>H3PO4>H2SO4 |
| B、氢化物的稳定性:H2S>HF>H2O |
| C、碱性:Al(OH)3>Mg(OH)2>NaOH |
| D、氧化性:F2>C12>Br2>I2 |
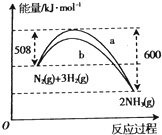 如图,a曲线是298K101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
如图,a曲线是298K101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 KJ/mol |
| B、b曲线是升高温度时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热减少 |
| D、在298K体积一定的条件下,通入1molN2和3molH2反应后放出的热量为Q1KJ,若通入2molN2和6molH2反应后放出的热量为Q2KJ,则184>Q2>2Q1 |
下列对实验仪器特点的描述正确的或实验能达到预期目的是( )
| A、用10mL量筒去量取7.50mL稀盐酸 |
| B、量筒的“0”刻度在下面 |
| C、托盘天平标尺的“0”刻度在中间 |
| D、用托盘天平称量25.5gNaCl晶体 |
下列物质既是钠盐,又是硫酸正盐的是( )
| A、NaHSO4 |
| B、Na2SO4 |
| C、Na2SO3 |
| D、Na2S2O3 |
氯气和亚硫酸钠间可发生氧化还原反应.将0.1molNa2SO3氧化成Na2SO4,至少需Cl2的物质的量为( )
| A、0.05 mol |
| B、0.1 mol |
| C、0.2 mol |
| D、0.4mol |


