题目内容
下列变化需克服相同类型作用力的是( )
| A、碘和干冰的升华 |
| B、硅和C60的熔化 |
| C、溴和汞的气化 |
| D、二氧化硅和铁分别受热熔化 |
考点:化学键和分子间作用力的区别
专题:
分析:题中碘、干冰、溴、C60属于分子晶体,汞、铁属于金属晶体,硅、二氧化硅属于原子晶体,以此判断.
解答:
解:A.碘和干冰属于分子晶体,升华时破坏分子间作用力,类型相同,故A正确;
B.硅属于原子晶体,C60属于分子晶体,熔化时分别破坏共价键和分子间作用力,故B错误;
C.溴气化破坏分子间作用力,汞气化破坏金属键,故C错误;
D.二氧化硅属于原子晶体,破坏共价键,铁气化破坏金属键,故D错误.
故选A.
B.硅属于原子晶体,C60属于分子晶体,熔化时分别破坏共价键和分子间作用力,故B错误;
C.溴气化破坏分子间作用力,汞气化破坏金属键,故C错误;
D.二氧化硅属于原子晶体,破坏共价键,铁气化破坏金属键,故D错误.
故选A.
点评:本题考查晶体的类型和微粒间作用力的判断,题目难度不大,注意物质发生变化时粒子间作用力的变化.

练习册系列答案
相关题目
关于如图所示装置的叙述,正确的是( )
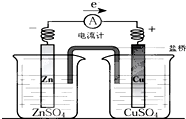

| A、铜是阳极,铜片上有气泡产生 |
| B、正极附近的SO42-离子浓度逐渐增大 |
| C、电流从锌片经导线流向铜片 |
| D、铜离子在铜片表面被还原 |
设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A、1.8 g的NH4+离子中含有的电子数为NA |
| B、常温常压下,11.2 L氧气所含的原子数为NA |
| C、常温常压下,48 g O3和O2的混合物含有的氧原子数为3NA |
| D、2.4 g金属镁变为镁离子时失去的电子数为0.2NA |
下列说法正确的是( )
| A、只有反应体系中所有分子同时都发生有效碰撞的反应才是放热反应 |
| B、通常条件下能够自发进行的反应必须具备△H和△S均大于0 |
| C、任何化学反应只要是自发进行的放热反应都可以设计成原电池,为外界提供电能 |
| D、实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配置氯化铁溶液 |
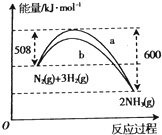 如图,a曲线是298K101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
如图,a曲线是298K101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 KJ/mol |
| B、b曲线是升高温度时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热减少 |
| D、在298K体积一定的条件下,通入1molN2和3molH2反应后放出的热量为Q1KJ,若通入2molN2和6molH2反应后放出的热量为Q2KJ,则184>Q2>2Q1 |
2012年2月新华网报道,加拿大开发出生产医用放射性同位素 9943Tc的简单方法.下列关的叙述正确的是( )
| A、原子序数是99 |
| B、质量数是43 |
| C、中子数是99 |
| D、电子数是43 |
下列对实验仪器特点的描述正确的或实验能达到预期目的是( )
| A、用10mL量筒去量取7.50mL稀盐酸 |
| B、量筒的“0”刻度在下面 |
| C、托盘天平标尺的“0”刻度在中间 |
| D、用托盘天平称量25.5gNaCl晶体 |