题目内容
3.在标准状况下,CO和CO2的混合气体共4.48L,质量为7.2g,则两种气体的物质的量之和为0.2mol,该混合气体的平均相对分子质量为36,其中CO2为4.4g.分析 根据n=$\frac{V}{Vm}$计算物质的量,根据总质量和总物质的量列式计算可得CO和CO2的质量,依据M=$\frac{m}{n}$计算混合气体平均相对分子质量.
解答 解:4.48L标况下气体物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,设CO物质的量为x,CO2物质的量为y,则x+y=0.2,28x+44y=7.2,解得x=0.1mol,y=0.1mol,则二氧化碳质量为0.1mol×44g/mol=4.4g;混合气体的平均摩尔质量为$\frac{7.2g}{0.2mol}$=36g/mol,所以相对分子质量为36;
故答案为:0.2;36;4.4.
点评 本题考查了物质的量相关计算,明确相关概念是解题关键,题目难度不大.

练习册系列答案
相关题目
13.下列说法不正确的是( )
| A. | 当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 | |
| B. | 将一块未擦去氧化膜的铝片分别投入1 mol•L-1 CuSO4溶液中,铝片表面观察不到明显的反应现象 | |
| C. | 制取摩尔盐时和制取阿司匹林时都可用酒精洗涤产品 | |
| D. | 在AlCl3溶液中先滴加足量的NH4F溶液,在滴加氨水,将看不到溶液变浑浊 |
14.下列溶液中氯离子浓度与50mL 1mol•L-1氯化铝溶液中氯离子浓度相等的是( )
| A. | 150 mL 1 mol•L-1氯化钠溶液 | B. | 150 mL 3 mol•L-1氯化钾溶液 | ||
| C. | 75 mL 2 mol•L-1氯化铵溶液 | D. | 50 mL 1 mol•L-1氯化铜溶液 |
18.下列判断正确的是( )
| A. | 原子半径:Cl>P | B. | 氢化物的稳定性:CH4<SiH4 | ||
| C. | 金属性强弱:Na>Li | D. | 酸性:H2CO3>H3PO4 |
8.某酸二酯(CPPO)的组成如图所示
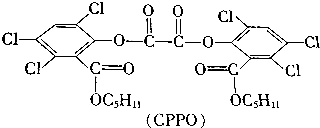
如果苯环上取代基位置和官能团位置都不改变,CPPO的结构有( )

如果苯环上取代基位置和官能团位置都不改变,CPPO的结构有( )
| A. | 32种 | B. | 36种 | C. | 64种 | D. | 72种 |
1.已知H-H、H-O和O═O键的键能分别为436kJ•mol-1,463kJ•mol-1,495kJ•mol-1,下列热化学方程式正确的是( )
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=-485 kJ•mol-1 | B. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=485 kJ•mol-1 | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=485 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-485 kJ•mol-1 |