题目内容
3.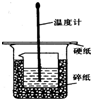 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中缺少的仪器是环形玻璃搅拌棒.
(2)指出该装置的一处错误大小烧杯之间没有填满碎纸条.
(3)实验中若用70mL0.50mol•L-1盐酸跟70mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量不相等 (填“相等”或“不相等”),所求中和热相等(填“相等”或“不相等”).
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会偏小(填“偏大”“偏小”或“无影响”).
分析 (1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(4)弱电解质电离吸收热量.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条,减少实验过程中的热量损失,
故答案为:大小烧杯之间没有填满碎纸条;
(3)反应放出的热量和所用酸以及碱的量的多少有关,并若用70mL0.50mol•L-1盐酸跟70mL0.55mol•L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用70mL0.50mol•L-1盐酸跟70mL0.55mol•L-1NaOH溶液进行反应,进行上述实验,测得中和热数值相等;
故答案为:不相等;相等;
(4)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于中和热数值,故答案为:偏小(4)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ;
故答案为:偏小.
点评 本题考查了中和热的测定方法、计算、误差分析,题目难度不大,注意掌握测定中和热的正确方法,明确实验操作过程中关键在于尽可能减少热量散失,使测定结果更加准确.

练习册系列答案
相关题目
13.一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(s)?zC(g),达到平衡后测得A气体的浓度为0.5mol•L-1,当恒温下将密闭容器的容积扩大到两倍再达到平衡后,测得A的浓度为0.3mol•L-1,则下列叙述正确的是( )
| A. | C的体积分数降低 | B. | x+y>z | ||
| C. | 平衡向正反应方向移动 | D. | x+y<z |
8.下列操作对中和滴定结果没有影响的是( )
| A. | 滴定管未用标准酸液或标准碱液润洗 | |
| B. | 锥形瓶用待测液润洗后加入待测液 | |
| C. | 滴定管在滴定前未进行赶气 | |
| D. | 读数时视线要平视 |
15.下列各元素的原子半径最大的是( )
| A. | F | B. | N | C. | O | D. | H |
13.下列各绸离子能在强酸性无色溶液中大量共存的是( )
| A. | Na+、K+、HCO3-、Cl- | B. | K+、NH4+、Cl-、SO42- | ||
| C. | K+、Cu2+、SO42、Cl- | D. | Mg2+、Cu2+、Cl-、NO3- |
 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应;通过测定反应过程中所放出的热量可计算中和反应热.
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应;通过测定反应过程中所放出的热量可计算中和反应热.