题目内容
11.现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2).已知实验中可能会发生下列反应:①2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
②3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
③2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C
④Mg+H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2↑
⑤Mg3N2+6H2O═3Mg(OH)2+2NH3↑
可供选择的装置和药品如下页图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连).
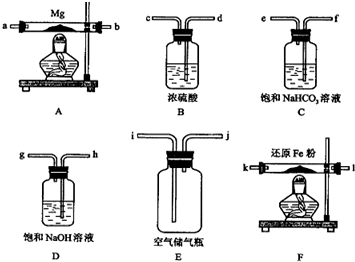
回答下列问题;
在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别为(可不填满)
| 装置 | 目的 |
(3)通气后,应先点燃F处的酒精灯,再点燃A处的酒精灯;如果同时点燃A、
F装置的酒精灯,对实验结果有何影响?制得的氮化镁不纯;
(4)请设计一个实验,验证产物是Mg3N2,写出操作步骤、现象和结论:将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁,若试纸不变蓝,则不含有Mg3N2.
分析 本题是在实验室里利用空气和镁粉为原料制取少量纯净的氮化镁,为了保证产品的纯度,需要除去空气中的氧气、二氧化碳及水气,分别利用还原铁粉、氢氧化钠溶液及浓硫酸完成,产品的检验可利用氮化镁的性质⑤来设计实验操作.
(1)根据题中信息可知Mg在空气中点燃可以和O2、CO2、H2O反应,所以镁和氮气反应必须将空气中的O2、CO2、H2O除去制得干燥纯净的N2,浓硫酸作用是除去水蒸气,浓氢氧化钠是除去空气中二氧化碳,灼热的铁粉为了除去空气中氧气;
(2)根据先除杂后干燥的原理及固体加热试管必须干燥的原理可将装置进行排序.气体参与的物质制备实验中装置的连接一般顺序是:制备气体→除杂→干燥→制备→尾气处理;
(3)通气后,先排除空气中的杂质,所以应该先点燃F;因为A装置没有排完空气前就加热会让空气中的氧气、CO2、水蒸气等与镁反应,如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁;
(4)取适量产物放入试管中,滴加蒸馏水,将润湿的红色石蕊试纸靠近试管口,如果试管中的溶液出现浑浊,红色石蕊试纸变蓝,则可以证明有氮化镁生成.
解答 解:(1)根据题中信息可知Mg在空气中点燃可以和O2、CO2、H2O反应,所以镁和氮气反应必须将空气中的O2、CO2、H2O除去制得干燥纯净的N2,浓硫酸作用是除去水蒸气,浓氢氧化钠是除去空气中二氧化碳,灼热的铁粉为了除去空气中氧气;所以在设计实验方案时,除装置A、E外,还应选择的装置B,目的是除气流中的水蒸汽,避免反应④发生;D,目的是除去空气中的CO2,避免反应③发生;F,目的是除去空气中的氧气,避免反应①发生,
故答案为:
| 装置 | 目的 |
| B | 目的是除气流中的水蒸汽,避免反应④发生 |
| D | 目的是除去空气中的CO2,避免反应③发生 |
| F | 目的是除去空气中的氧气,避免反应①发生 |
故答案为:j→h→g→d→c→k→l(或l→k)→a→b (或b→a);
(3)通气后,先排除空气中的杂质,所以应该先点燃F,再点燃F,因为A装置没有排完空气前就加热会让空气中的氧气、CO2、水蒸气等与镁反应,如果装置F中的还原铁粉没有达到反应温度时,氧气不能除尽,导致氧同镁反应,而使氮化镁中混入氧化镁;
故答案为:F;A;制得的氮化镁不纯;
(4)依据氮化镁和水反应生成氨气,方程式为 Mg3N2+6H2O=3Mg(OH)2+2NH3↑,将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁,
故答案为:将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁,若试纸不变蓝,则不含有Mg3N2.
点评 本题考查了物质制备原理和装置选择,实验步骤的设计分析判断、物质性质的应用是解题的关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | NaHSO3溶液与NaOH溶液反应:HSO3-+OH-═SO32-+H2O | |
| B. | 少量二氧化碳通入足量的NaOH溶液:CO2+2OH-═CO32-+H2O | |
| C. | Ba(OH)2与H2SO4反应:H++OH-═H2O | |
| D. | 氨水和醋酸溶液混合:NH3•H2O+CH3COOH═NH4++CH3COO-+H2O |

 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O.
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O.
 .
.