题目内容
19.关于Na2CO3和NaHCO3的叙述正确的是( )| A. | NaHCO3和Na2CO3均能和BaCl2反应 | |
| B. | NaHCO3和Na2CO3都能加热分解,产生使石灰水变浑浊的气体 | |
| C. | 质量相同的NaHCO3和Na2CO3分别与足量稀盐酸反应,NaHCO3放出气体多 | |
| D. | 可以用澄清石灰水来鉴别Na2CO3NaHCO3溶液 |
分析 A、NaHCO3和BaCl2不反应;
B、NaHCO3受热分解,Na2CO3而受热不分解;
C、利用n=$\frac{m}{M}$,可计算物质的量,因酸足量,利用Na2CO3~CO2,NaHCO3~CO2来分析;
D、Na2CO3和NaHCO3溶液都与澄清石灰水反应生成碳酸钙.
解答 解:A、NaHCO3和BaCl2不符合复分解反应的条件,所以两者不反应,故A错误;
B、NaHCO3受热分解产生使石灰水变浑浊的气体,Na2CO3而受热不分解,故B错误;
C、设质量都是106g,则Na2CO3和NaHCO3的物质的量分别为1mol、$\frac{106}{84}$mol,根据Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol、$\frac{106}{84}$mol,故C正确;
D、Na2CO3和NaHCO3溶液都与澄清石灰水反应生成碳酸钙,所以不能用澄清石灰水来鉴别,故D错误;
故选C.
点评 本题考查碳酸钠和碳酸氢钠的性质,涉及溶解度、稳定性、与酸的反应等,注意与酸反应中量少的物质完全反应,题目难度不大.

练习册系列答案
相关题目
13.把pH=13的NaOH溶液与pH=2的硫酸溶液混合后,所得溶液的pH=11,则NaOH溶液和硫酸溶液的体积之比为( )
| A. | 1:1 | B. | 1:5 | C. | 1:9 | D. | 2:3 |
10.用如图所示装置进行实验.能形成‘喷泉”的气体是( )
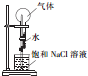

| A. | O2 | B. | Cl2 | C. | HCl | D. | N2 |
7.下列各组物质中,属于同素异形体的是( )
| A. | 红磷和白磷 | B. | 冰和干冰 | C. | NH3和NH4+ | D. | O2和O2- |
4.下列实验现象和结论或原因相符的是( )
| 操作及现象 | 原因或结论 | |
| A | 一块表面打磨过的铝箔在酒精灯上加热至熔化,液态铝不会滴落. | 铝的熔点高于三氧化二铝 |
| B | 某溶液中加入硝酸银,产生白色沉淀 | 溶液中一定含有Cl- |
| C | 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 溶液中有Na+,无K+ |
| D | 向某溶液中先加KSCN无明显现象,再滴氯水,溶液变红 | 溶液中一定含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
11.下列离子方程式书写正确的是( )
| A. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 以石墨作电极电解氯化铝溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| D. | FeBr2与等物质的量的Cl2反应:2Fe2++4Br-+3Cl2═2Fe3++6Cl-+2Br2 |
8.铂金色泽淡雅而华贵,象征着纯洁与高尚,近年来铂金饰品越来越受到人们宠爱.我国科学家在世界上首次发现铂的一种新核素${\;}_{78}^{202}$Pt,下列说法正确的是( )
| A. | ${\;}_{78}^{202}$Pt原子核中含有78个中子 | |
| B. | ${\;}_{78}^{202}$Pt原子核外有124个电子 | |
| C. | ${\;}_{78}^{195}$Pt和${\;}_{78}^{202}$Pt互为同素异形体 | |
| D. | ${\;}_{78}^{195}$Pt和${\;}_{78}^{202}$Pt互为同位素 |
9.下列有关元素或者化合物性质的比较中,正确的是( )
| A. | 结构相似的分子晶体的溶沸点,与相对分子质量呈正相关,所以HF<HCl | |
| B. | Na、Mg、Al原子最外层电子数依次增多,原子半径也依次增大 | |
| C. | 在分子中,两个原子间的键长越长,键能越大 | |
| D. | 一般而言,晶格能越高,离子晶体的熔点越高、硬度越大 |