题目内容
7.下列各组物质中,属于同素异形体的是( )| A. | 红磷和白磷 | B. | 冰和干冰 | C. | NH3和NH4+ | D. | O2和O2- |
分析 由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.
解答 解:A.红磷和白磷都是由同种元素形成的不同物质,都是单质,互为同素异形体,故A正确;
B.冰和干冰是化合物,不是单质,故B错误;
C.NH3和NH4+不是单质,故C错误;
D.O2-不是单质,故D错误.
故选A.
点评 本题考查同素异形体,难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,②不同单质,这是解决此类题的关键之所在.

练习册系列答案
相关题目
1.下列晶胞所对应的化学式正确的是( )
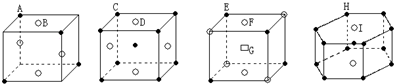

| A. | A3B4 | B. | CD | C. | EF3G2 | D. | H5I |
2.下列实验装置或实验方案能达到目的是( )
| A. | 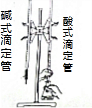 用HF标准溶液测定未知浓度的NaOH溶液 用HF标准溶液测定未知浓度的NaOH溶液 | |
| B. | 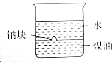 验证密度:ρ(水)<ρ(钠)<ρ(煤油) 验证密度:ρ(水)<ρ(钠)<ρ(煤油) | |
| C. | 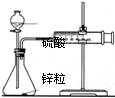 测定锌与硫酸反应的速率 测定锌与硫酸反应的速率 | |
| D. | 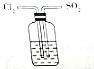 验证SO2和Cl2等物质的量混合增强漂白效果 验证SO2和Cl2等物质的量混合增强漂白效果 |
15.下列说法中,正确的是( )
| A. | 有机物和无机物都只能从有机体内提取 | |
| B. | 有机物都难溶于水,无机物都易溶于水 | |
| C. | 用化学方法能合成自然界已存在或不存在的有机物 | |
| D. | 有机物参与的反应速率一定比无机物参与的反应慢,且常伴有副反应 |
2.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 一定条件下,1 mol N2与足量H2反应生成NH3,转移电子6NA | |
| C. | pH=13的氢氧化钠溶液中所含Na+为0.1NA | |
| D. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
19.关于Na2CO3和NaHCO3的叙述正确的是( )
| A. | NaHCO3和Na2CO3均能和BaCl2反应 | |
| B. | NaHCO3和Na2CO3都能加热分解,产生使石灰水变浑浊的气体 | |
| C. | 质量相同的NaHCO3和Na2CO3分别与足量稀盐酸反应,NaHCO3放出气体多 | |
| D. | 可以用澄清石灰水来鉴别Na2CO3NaHCO3溶液 |
16.能用共价键键能大小解释的是( )
| A. | 还原性:HI>HF | B. | 溶解度:HF>HI | C. | 沸点:HF>HI | D. | 分解温度:HF>HI |
17.常温下,下列说法不正确的是( )
| A. | 在0.1mol/L的HNO3溶液中由水电出的c(H+)<$\sqrt{{K}_{W}}$ | |
| B. | 常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c (Na+)=c(CH3COO-) | |
| C. | 向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) |
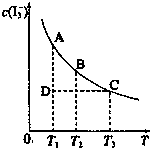 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I-3(aq).I2、KI混合溶液中,I-3的物质的量浓度c(I-3)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下到说法正确的组合是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I-3(aq).I2、KI混合溶液中,I-3的物质的量浓度c(I-3)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下到说法正确的组合是( )