题目内容
9.下列说法错误的是( )| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 共价化合物中一定没有离子键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 双原子单质分子中的共价键一定是非极性键 |
分析 A.离子化合物中一定含有离子键,可能含有共价键;
B.只含共价键的化合物是共价化合物;
C.含有共价键的化合物可能是离子化合物;
D.同种非金属元素之间易形成非极性共价键.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,所以含有离子键的化合物的离子化合物,故A正确;
B.只含共价键的化合物是共价化合物,离子化合物中一定不含离子键,故B正确;
C.含有共价键的化合物可能是离子化合物,如KOH等,故C错误;
D.同种非金属元素之间易形成非极性共价键,所以双原子单质分子中的共价键一定是非极性键,故D正确;
故选C.
点评 本题考查化合物和化学键的关系,明确物质的构成微粒即可判断化学键,注意离子键化合物和共价化合物的根本区别,不能根据是否含有金属元素判断离子化合物.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.向盐酸中加入浓硫酸时产生白雾,下列叙述不属于产生该现象的原因是( )
| A. | 浓硫酸具有脱水性 | B. | 浓硫酸具有吸水性 | ||
| C. | 盐酸具有挥发性 | D. | 气体的溶解度的随温度升高而降低 |
4.节日里,小朋友们玩的荧光棒的发光原理是:化学物质相互反应过程中,能量以光的形式释放出来.发荧光棒放在热水中,荧光棒会更亮,原因之一是( )
| A. | 反应物浓度减小,反应速率减小 | |
| B. | 反应物浓度增加,反应速率增加 | |
| C. | 温度升高,反应速率增加 | |
| D. | 热水对反应起催化作用,从而加快了反应速率 |
14.元素X的原子核外M电子层上有3个电子,元素Y2-的离子核外有18个电子,则这两种元素可形成的化合物为( )
| A. | XY2 | B. | X2Y3 | C. | X3Y2 | D. | X2Y |
1.类比推理是化学学习中的一种重要方法.下列类推结论正确的是( )
| 类比对象 | 结论 | |
| A | Cl2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$HCl+HClO | I2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$HI+HIO |
| B | C+2CuO$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2↑ | C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ |
| C | Na2O+H2O=2NaOH | CuO+H2O=Cu(OH)2 |
| D | Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
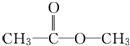 、
、 或
或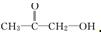 .
.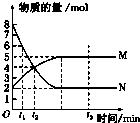 一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示: