题目内容
五种短周期元素A、B、C、D、E的原子序数依次增大.A、B、C三种元素原子核外电子层数之和是5.A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外层上的电子数是其电子层数的2倍,A和C可以形成化合物CA3;B与D的原子序数之比为3:4;E元素原子最外层电子数比次外层电子数少1.
(1)D元素在周期表中的位置 ;CE3的结构式为 ;由A、B、D三种元素组成的18电子微粒的电子式为 .
(2)B元素形成的同素异形体的晶体类型可能是
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)由A分别和B、C、D所形成的常见共价化合物中,热稳定性最好的是 (填物质的化学式),该化合物的空间构型为 .
(4)ED2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可用KED3和草酸在稀硫酸酸化的环境中反应制得气体ED2,试写出该反应的离子方程式并配平: .
(1)D元素在周期表中的位置
(2)B元素形成的同素异形体的晶体类型可能是
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)由A分别和B、C、D所形成的常见共价化合物中,热稳定性最好的是
(4)ED2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可用KED3和草酸在稀硫酸酸化的环境中反应制得气体ED2,试写出该反应的离子方程式并配平:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:五种短周期元素A、B、C、D、E的原子序数依次增大.B元素原子最外层上的电子数是其电子层数的2倍,则B原子有2个电子层,最外层电子数为4,则B为碳元素;A、B、C三种元素原子核外电子层数之和是5,结合原子序数可知,A处于第一周期,则A为氢元素,C处于第二周期,A、B两元素原子最外层电子数之和等于C元素原子最外层电子数,则C原子最外层电子数为1+4=5,故C为氮元素,A和C可以形成化合物NH3;B与D的原子序数之比为3:4,则D的原子序数为8,故D为氧元素;E元素原子最外层电子数比次外层电子数少1,原子序数大于O元素,处于第三周期,则E最外层电子数为7,为Cl元素,据此解答.
解答:
解:依据分析可知:A为H,B为C,C为N,D为O,E为Cl,
(1)O元素位于第二周期第ⅥA组族,NCl3的结构类似于氨气,故式NCl3的结构式为: ,C、H、O三种元素组成的18电子微粒为甲醇,电子式为:
,C、H、O三种元素组成的18电子微粒为甲醇,电子式为: ,故答案为:第二周期第ⅥA组族;
,故答案为:第二周期第ⅥA组族; ;
; ;
;
(2)C元素形成的同素异形体为金刚石或C60,金刚石为原子晶体,C60为分子晶体晶体,故答案为:①③;
(3)由H分别和C、N、O所形成的常见共价化合物为甲烷、氨气和水,由于水分子中存在氢键,故水的热稳定性最好,水的空间构型为V型,故答案为:H2O;V型;
(4)ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可用KClO3和草酸在稀硫酸酸化的环境中反应制得气体ClO2,该反应的离子反应方程式为:2ClO3-+H2C2O4+2H+=2ClO2↑+2CO2↑+2H2O,故答案为:2ClO3-+H2C2O4+2H+=2ClO2↑+2CO2↑+2H2O.
(1)O元素位于第二周期第ⅥA组族,NCl3的结构类似于氨气,故式NCl3的结构式为:
 ,C、H、O三种元素组成的18电子微粒为甲醇,电子式为:
,C、H、O三种元素组成的18电子微粒为甲醇,电子式为: ,故答案为:第二周期第ⅥA组族;
,故答案为:第二周期第ⅥA组族; ;
; ;
;(2)C元素形成的同素异形体为金刚石或C60,金刚石为原子晶体,C60为分子晶体晶体,故答案为:①③;
(3)由H分别和C、N、O所形成的常见共价化合物为甲烷、氨气和水,由于水分子中存在氢键,故水的热稳定性最好,水的空间构型为V型,故答案为:H2O;V型;
(4)ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可用KClO3和草酸在稀硫酸酸化的环境中反应制得气体ClO2,该反应的离子反应方程式为:2ClO3-+H2C2O4+2H+=2ClO2↑+2CO2↑+2H2O,故答案为:2ClO3-+H2C2O4+2H+=2ClO2↑+2CO2↑+2H2O.
点评:本题主要考查的是元素的推断依据元素化合物知识,正确书写离子反应方程式等是关键,属于常考题.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
一定条件下,在体积为2L的密闭容器中,3molX和3mol Y发生反应:3X(g)+Y(g)═2Z(g),经60s达到平衡,生成0.4molZ.下列说法正确的是( )
| A、60s内反应速率为v(X)=0.05 mol/(L?s),X的转化率为80% | ||
B、其它条件不变,将容器体积变为4L,Z的平衡浓度变为原来的
| ||
| C、其它条件不变,若升高温度,X的体积分数增大,则该反应的△H>0 | ||
| D、其它条件不变,若初始投入2mol X和2mol Y则物质Y的转化率减小 |
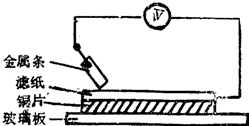 如图所示实验中,把四根洁净的金属条A、B、C、D轮流放置在浸有盐溶液的滤纸上面并压紧.在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如下表).下列说法中正确的是( )
如图所示实验中,把四根洁净的金属条A、B、C、D轮流放置在浸有盐溶液的滤纸上面并压紧.在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如下表).下列说法中正确的是( )| 金属 | 电子流动方向 | 电压 |
| A | A→Cu | +0.78 |
| B | Cu→B | -2.15 |
| C | C→Cu | +1.35 |
| D | +0.30 |
| A、金属D与Cu之间电子流动方向为Cu→D |
| B、A金属可能是最强的还原剂 |
| C、B金属不能从硫酸铜溶液中置换铜 |
| D、B金属可能是最强的还原剂 |
下列离子方程式中正确的是( )
| A、稀硫酸与氢氧化钡溶液反应Ba2++SO42-=BaSO4↓ |
| B、铝与氢氧溶液化钠反应Al+2OH-=AlO2-+H2↑ |
| C、向Na2CO3浓溶液中缓慢滴加几滴稀盐酸CO32-+H+=HCO3- |
| D、锌粒与稀醋酸反应Zn+2H+=Zn2++H2↑ |

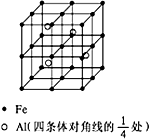 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.