题目内容
一定条件下,在体积为2L的密闭容器中,3molX和3mol Y发生反应:3X(g)+Y(g)═2Z(g),经60s达到平衡,生成0.4molZ.下列说法正确的是( )
| A、60s内反应速率为v(X)=0.05 mol/(L?s),X的转化率为80% | ||
B、其它条件不变,将容器体积变为4L,Z的平衡浓度变为原来的
| ||
| C、其它条件不变,若升高温度,X的体积分数增大,则该反应的△H>0 | ||
| D、其它条件不变,若初始投入2mol X和2mol Y则物质Y的转化率减小 |
考点:化学平衡的计算
专题:
分析:经60s达到平衡,正反应速率等于逆反应速率,达到平衡之后,如外界条件不不变,则平衡状态不变,正逆反应速率相等,结合生成Z的物质的量进行相关的计算.
解答:
解:A、经60s达到平衡,生成0.4molZ,则v(Z)=
=
mol/(L?s),故v(X)=
v(Z)=
=0.005mol/(L?s),故A错误;
B、其它条件不变,将容器体积变为4L,Z的平衡浓度瞬间变为原来的
,但是此时由于减小压强,故平衡左移,导致Z的浓度继续降低,故B错误;
C、其它条件不变,若升高温度,X的体积分数增大,那么平衡左移,即升高温度,平衡向着吸热反应方向移动,故则该反应的逆反应吸热,那么正反应放热,即△H<0,故C错误;
D、其它条件不变,若初始投入2mol X和2mol Y,对比3molX和3molY,相当于降低了体系的压强,故平衡左移,即Y的转化率减小,故D正确,故选D.
| ||
| 60s |
| 1 |
| 300 |
| 3 |
| 2 |
| 1 |
| 200 |
B、其它条件不变,将容器体积变为4L,Z的平衡浓度瞬间变为原来的
| 1 |
| 2 |
C、其它条件不变,若升高温度,X的体积分数增大,那么平衡左移,即升高温度,平衡向着吸热反应方向移动,故则该反应的逆反应吸热,那么正反应放热,即△H<0,故C错误;
D、其它条件不变,若初始投入2mol X和2mol Y,对比3molX和3molY,相当于降低了体系的压强,故平衡左移,即Y的转化率减小,故D正确,故选D.
点评:本题考查化学平衡问题,题目难度不大,本题注意外界条件对化学平衡的影响,根据化学反应速率之比等于化学质量数之比计算反应速率.

练习册系列答案
相关题目
化肥和农药对农牧业的增产增收起重要作用,但使用不当也会给人类和环境带来危害.下列关化肥或农药的使用描述不正确的是( )
| A、(NH4)2SO4的大量使用可能造成土壤的碱化 |
| B、磷肥的大量使用可能造成水体富营养化 |
| C、农药的使用可能影响害虫与其天敌之间的生态平衡 |
| D、家蚕吞食喷洒过农药的桑叶,可能引起中毒 |
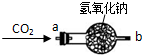 某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.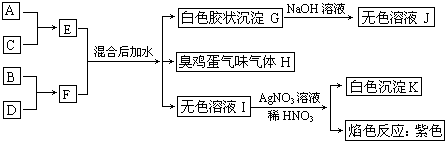


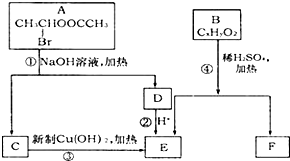 已知一个碳原子上连有两个羟基时,易发生下列转化:
已知一个碳原子上连有两个羟基时,易发生下列转化: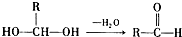
 第45届世界体操锦标赛于2014年10月3日至12日在广西体育中心体育馆举行.
第45届世界体操锦标赛于2014年10月3日至12日在广西体育中心体育馆举行.