题目内容
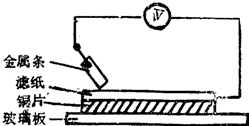 如图所示实验中,把四根洁净的金属条A、B、C、D轮流放置在浸有盐溶液的滤纸上面并压紧.在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如下表).下列说法中正确的是( )
如图所示实验中,把四根洁净的金属条A、B、C、D轮流放置在浸有盐溶液的滤纸上面并压紧.在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如下表).下列说法中正确的是( )| 金属 | 电子流动方向 | 电压 |
| A | A→Cu | +0.78 |
| B | Cu→B | -2.15 |
| C | C→Cu | +1.35 |
| D | +0.30 |
| A、金属D与Cu之间电子流动方向为Cu→D |
| B、A金属可能是最强的还原剂 |
| C、B金属不能从硫酸铜溶液中置换铜 |
| D、B金属可能是最强的还原剂 |
考点:验证原电池的效果
专题:
分析:根据原电池中电子的流向判断金属的强弱,电压值越大,金属的活泼性越强,
A、金属A与Cu形成的电压为+,说明金属D比Cu活泼,电子流动方向为A→Cu;
B、电压值越大,金属的活泼性越强,金属的还原性越强;
C、电压为-,说明Cu比金属B活泼,因此金属B金属不能从硫酸铜溶液中置换铜;
D、B金属对应的电压最小,说明B金属是还原性最弱的金属.
A、金属A与Cu形成的电压为+,说明金属D比Cu活泼,电子流动方向为A→Cu;
B、电压值越大,金属的活泼性越强,金属的还原性越强;
C、电压为-,说明Cu比金属B活泼,因此金属B金属不能从硫酸铜溶液中置换铜;
D、B金属对应的电压最小,说明B金属是还原性最弱的金属.
解答:
解:A、金属A与Cu形成的电压为+,说明金属D比Cu活泼,电子流动方向为A→Cu,故A错误;
B、电压值越大,金属的活泼性越强,金属的还原性越强,因此最强的还原剂为金属C,故B错误;
C、电压为-,说明Cu比金属B活泼,因此金属B金属不能从硫酸铜溶液中置换铜,故C正确;
D、B金属对应的电压最小,说明B金属是还原性最弱的金属,故D错误;
故选C.
B、电压值越大,金属的活泼性越强,金属的还原性越强,因此最强的还原剂为金属C,故B错误;
C、电压为-,说明Cu比金属B活泼,因此金属B金属不能从硫酸铜溶液中置换铜,故C正确;
D、B金属对应的电压最小,说明B金属是还原性最弱的金属,故D错误;
故选C.
点评:本题考查常见金属的活动性顺序的比较方法以及金属的电化学腐蚀及防护,题目难度中等,注意把握原电池的工作原理,注意加强对数据分析能力的培养.

练习册系列答案
相关题目
存在如下三个反应:①PCl5(g)?PCl 3(g)+Cl2(g) ②2HI(g)?H2(g)+I2(g)③2NO2(g)?N2O4(g)在一定条件下,以上三个反应达到化学平衡时,反应物的转化率均是b%.若保持恒温恒容,分别再加入一定量的各自的反应物,则转化率( )
| A、均减少 |
| B、均增大 |
| C、①增大,②不变,③减少 |
| D、①减少,②不变,③增大 |
某溶液中加入BaCl2溶液,生成不溶于稀盐酸的白色沉淀,则溶液中溶有的离子是( )
| A、一定溶有CO32- |
| B、一定溶有SO42- |
| C、一定溶有Ag+ |
| D、可能溶有SO42-或Ag+ |
某无色溶液中能大量共存的一组离子是( )
| A、OH-、Ba2+、HCO3-、Cl- |
| B、K+、Fe2+、H+、NO3- |
| C、NH4+、Al3+、Cl-、NO3- |
| D、Mg2+、SO42-、SiO32-、H+ |
结构简式为(CH3)3CCH2CH3的烷烃,进行二氯取代反应后,生成的二氯取代产物有( )(不考虑立体异构)
| A、6种 | B、7种 | C、8种 | D、9种 |
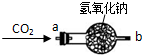 某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.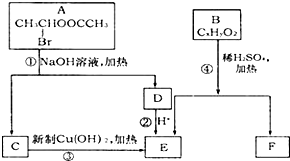 已知一个碳原子上连有两个羟基时,易发生下列转化:
已知一个碳原子上连有两个羟基时,易发生下列转化: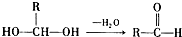
 第45届世界体操锦标赛于2014年10月3日至12日在广西体育中心体育馆举行.
第45届世界体操锦标赛于2014年10月3日至12日在广西体育中心体育馆举行.