题目内容
铜在一定条件也会生锈,其主要成分是铜绿,化学式为Cu2(OH)nCO3,式中n等于( )
| A、1 | B、2 | C、3 | D、4 |
考点:根据化学式判断化合价
专题:原子组成与结构专题
分析:Cu2(OH)nCO3中Cu为+2价,0H-为-1价,CO32-为-2价,根据化合物中正负化合价的代数和等于0计算出n值.
解答:
解:Cu2(OH)nCO3中Cu为+2价,0H-为-1价,CO32-为-2价,根据化合物中正负化合价的代数和等于0得:
2×2+(-1)×n+(-2)=0,解得n=2,
故选B.
2×2+(-1)×n+(-2)=0,解得n=2,
故选B.
点评:本题考查了化合物中化合价之和等于0这一重要性质,熟悉常见元素的化合价及化合价原则即可解答,较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200℃左右供电.电池总反应为:C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( )
美国圣路易斯大学研制新型的乙醇燃料电池,用质子(H+)溶剂,在200℃左右供电.电池总反应为:C2H5OH+3O2→2CO2+3H2O,如图是该电池的示意图,下列说法正确的是( )| A、a极为电池的正极 |
| B、电池工作时电流由a极沿导线经灯泡再到b极 |
| C、电池正极的电极反应为:4H++O2+4e-═2H2O |
| D、电池工作时,1mol乙醇被氧化时就有6mol电子转移 |
下列各组物质中,互为同分异构体的是( )
| A、冰和水 |
| B、氧气和臭氧 |
| C、1H与3H |
| D、CH3CH20H和CH30CH3 |
常温下,pH=11的氨水和pH=1的盐酸等体积混合(混合溶液体积为两溶液体积之和),恰好完全中和,则下列说法错误的是( )
| A、氨水的浓度等于盐酸的浓度 |
| B、原氨水中有1%的含氮微粒为NH4+ |
| C、氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
| D、混合溶液中c(NH4+)+c(NH3?H2O)+c(NH3)=5×10-4mol?L-1 |
X、Y、Z、W是前20号元素,原子序数依次增大.X是原子半径最小的元素;Y元素原子的最外层电子数是电子层数的2倍;Z元素的-1价阴离子的核外电子排布与氖原子相同,W元素为金属,它的某种化合物可用于烟气脱硫.下列说法错误的是( )
| A、X、Y形成的化合物中可能含有双键 |
| B、X单质和Z单质在暗处能剧烈反应 |
C、W元素与Z元素形成的化合物用电子式表示形成过程为: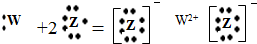 |
| D、XZ的沸点在与Z同族的其它X的化合物中最高 |
下列有关离子(或物质)的检验及结论正确的是( )
| A、用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定不含有K+ |
| B、向无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀出现,则溶液中含有SO42ˉ |
| C、向某溶液中滴加少量氯水,再滴加KSCN溶液,若溶液变成血红色,则原溶液中一定有Fe2+ |
| D、向某黄色溶液中加入淀粉溶液,若溶液变蓝色,则原溶液中含有I2 |
下列有关电化学装置的说法正确的是( )
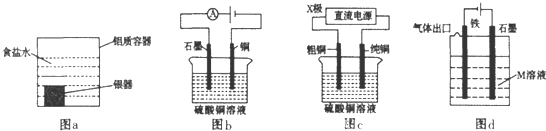

| A、利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为Ag2S+2e-=2Ag+S2- |
| B、图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出 |
| C、图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D、图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
 下表是在0.1MPa下,不同温度时,二氧化硫催化氧化成三氧化硫的平衡转化率(原料气成分的体积分数:SO27%,O211%,N282%):
下表是在0.1MPa下,不同温度时,二氧化硫催化氧化成三氧化硫的平衡转化率(原料气成分的体积分数:SO27%,O211%,N282%):