题目内容
 下表是在0.1MPa下,不同温度时,二氧化硫催化氧化成三氧化硫的平衡转化率(原料气成分的体积分数:SO27%,O211%,N282%):
下表是在0.1MPa下,不同温度时,二氧化硫催化氧化成三氧化硫的平衡转化率(原料气成分的体积分数:SO27%,O211%,N282%):| 温度/℃ | 400 | 450 | 475 | 500 | 525 | 575 |
| 转化率/% | 99.2 | 97.5 | 95.8 | 93.5 | 90.5 | 79.9 |
(1)根据表中信息可知,该可逆反应正反应的△H
理由是
(2)下列措施既能加快该反应的速率,又能提高二氧化硫转化率的是
A.选用更有效的催化剂B.充入更多的氧气
C.降低反应体系的温度D.缩小容器的体积
(3)为了探究O2的体积分数及压强对SO3含量的影响,某同学在同一密闭容器中进行下列三组实验.
| 实验 编号 |
压强(MPa) | SO2初始体积分数 (%) |
O2初始体积分数 (%) |
N2初始体积分数 (%) |
| Ⅰ | 0.1 | 7% | 11% | 82% |
| Ⅱ | ① | 7% | 15% | ② |
| Ⅲ | 0.5 | ③ | 15% | ④ |
考点:化学平衡的影响因素,体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:(1)由表中数据可知,温度越高,二氧化硫的转化率越低,说明升高温度平衡向逆反应方向移动;
(2)A.选用更有效的催化剂,加快反应速率,不影响平衡移动;
B.充入更多的氧气,反应速率加快,有利于平衡向正反应方向移动;
C.降低反应体系的温度,反应速率降低,平衡向放热反应方向移动,结合反应热效应判断;
D.缩小容器的体积,压强增大,反应速率增大,平衡向气体体积减小的方向移动;
(3)实验目的是:为了探究O2的体积分数及压强对SO3含量的影响,应采取控制变量法进行实验:
对比Ⅰ、Ⅱ可知,O2初始体积分数不同,应是探究O2的体积分数对SO3含量的影响,两组中压强、氮气的体积分数应相同;
对比Ⅱ、Ⅲ可知.O2初始体积分数相同,应是探究压强对SO3含量的影响,两组中SO2、N2的初始体积分数应相同;
实验Ⅰ与实验Ⅱ相比,实验Ⅰ中氧气的体积分数小,氧气的浓度小,反应速率较慢,到达平衡时间较实验Ⅱ长,不利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中低;
Ⅲ与实验Ⅱ相比,实验Ⅲ中压强高,反应速率快,到达平衡时间段,压强大,有利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中高.
(2)A.选用更有效的催化剂,加快反应速率,不影响平衡移动;
B.充入更多的氧气,反应速率加快,有利于平衡向正反应方向移动;
C.降低反应体系的温度,反应速率降低,平衡向放热反应方向移动,结合反应热效应判断;
D.缩小容器的体积,压强增大,反应速率增大,平衡向气体体积减小的方向移动;
(3)实验目的是:为了探究O2的体积分数及压强对SO3含量的影响,应采取控制变量法进行实验:
对比Ⅰ、Ⅱ可知,O2初始体积分数不同,应是探究O2的体积分数对SO3含量的影响,两组中压强、氮气的体积分数应相同;
对比Ⅱ、Ⅲ可知.O2初始体积分数相同,应是探究压强对SO3含量的影响,两组中SO2、N2的初始体积分数应相同;
实验Ⅰ与实验Ⅱ相比,实验Ⅰ中氧气的体积分数小,氧气的浓度小,反应速率较慢,到达平衡时间较实验Ⅱ长,不利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中低;
Ⅲ与实验Ⅱ相比,实验Ⅲ中压强高,反应速率快,到达平衡时间段,压强大,有利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中高.
解答:
解:(1)由表中数据可知,升高温度,二氧化硫的转化率越低,说明平衡向逆反应方向移动,正反应为放热反应,即△H<0,
故答案为:<;升高温度,二氧化硫的转化率越低,说明平衡向逆反应方向移动,正反应为放热反应;
(2)A.选用更有效的催化剂,加快反应速率,不影响平衡移动,二氧化硫转化率不变,故A错误;
B.充入更多的氧气,反应速率加快,有利于平衡向正反应方向移动,二氧化硫转化率增大,故B正确;
C.正反应为放热反应,降低反应体系的温度,平衡向正反应方向移动,二氧化硫转化率增大,但反应速率降低,故C错误;
D.缩小容器的体积,压强增大,反应速率加快,正反应为气体体积减小的反应,平衡向正反应方向移动,二氧化硫转化率增大,故D正确,
故答案为:BD;
(3)实验目的是:为了探究O2的体积分数及压强对SO3含量的影响,应采取控制变量法进行实验:
对比Ⅰ、Ⅱ可知,O2初始体积分数不同,应是探究O2的体积分数对SO3含量的影响,两组中压强、氮气的体积分数应相同,故①=0.1、②=82%;
对比Ⅱ、Ⅲ可知.O2初始体积分数相同,应是探究压强对SO3含量的影响,两组中SO2、N2的初始体积分数应相同,故③=7%、④=82%;
实验Ⅰ与实验Ⅱ相比,实验Ⅰ中氧气的体积分数小,氧气的浓度小,反应速率较慢,到达平衡时间较实验Ⅱ长,不利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中低;Ⅲ与实验Ⅱ相比,实验Ⅲ中压强高,反应速率快,到达平衡时间段,压强大,有利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中高,故Ⅰ、Ⅲ实验时混合气体中SO3的体积分数随时间变化的曲线图为: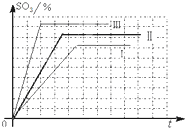 ,
,
故答案为:①=0.1;②=82%;③=7%;④=82%; .
.
故答案为:<;升高温度,二氧化硫的转化率越低,说明平衡向逆反应方向移动,正反应为放热反应;
(2)A.选用更有效的催化剂,加快反应速率,不影响平衡移动,二氧化硫转化率不变,故A错误;
B.充入更多的氧气,反应速率加快,有利于平衡向正反应方向移动,二氧化硫转化率增大,故B正确;
C.正反应为放热反应,降低反应体系的温度,平衡向正反应方向移动,二氧化硫转化率增大,但反应速率降低,故C错误;
D.缩小容器的体积,压强增大,反应速率加快,正反应为气体体积减小的反应,平衡向正反应方向移动,二氧化硫转化率增大,故D正确,
故答案为:BD;
(3)实验目的是:为了探究O2的体积分数及压强对SO3含量的影响,应采取控制变量法进行实验:
对比Ⅰ、Ⅱ可知,O2初始体积分数不同,应是探究O2的体积分数对SO3含量的影响,两组中压强、氮气的体积分数应相同,故①=0.1、②=82%;
对比Ⅱ、Ⅲ可知.O2初始体积分数相同,应是探究压强对SO3含量的影响,两组中SO2、N2的初始体积分数应相同,故③=7%、④=82%;
实验Ⅰ与实验Ⅱ相比,实验Ⅰ中氧气的体积分数小,氧气的浓度小,反应速率较慢,到达平衡时间较实验Ⅱ长,不利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中低;Ⅲ与实验Ⅱ相比,实验Ⅲ中压强高,反应速率快,到达平衡时间段,压强大,有利于平衡向正反应进行,平衡时SO3含量较实验Ⅱ中高,故Ⅰ、Ⅲ实验时混合气体中SO3的体积分数随时间变化的曲线图为:
 ,
,故答案为:①=0.1;②=82%;③=7%;④=82%;
 .
.
点评:本题考查化学平衡及反应速率影响因素、控制变量法探究外界条件对物质转化率的影响等,难度中等,(3)中注意根据控制变量法进行分析解答,作图时注意到达平衡时间与三氧化硫的含量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为36,原子最外层电子数之和为14.其中A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数.下列叙述正确的是( )
| A、一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
| B、D元素处于元素周期表中第3周期第IVA族 |
| C、A、C的最高价氧化物均为离子化合物 |
| D、四种元素的原子半径:A>B>D>C |
下列说法正确的是( )
| A、所有化学变化一定遵循质量守恒和能量守恒 |
| B、所有化学变化的能量都可以通过原电池转化为电能 |
| C、化学键的变化必然会引起能量变化,所以,能量变化也一定会引起化学变化 |
| D、断开旧化学键与形成新化学键之间的能量差只能以热量的形式释放 |
铜在一定条件也会生锈,其主要成分是铜绿,化学式为Cu2(OH)nCO3,式中n等于( )
| A、1 | B、2 | C、3 | D、4 |
 X、Y、Z、W四种短周期元素在元素周期表的位置如图.其中W的原子序数是Y的2倍.
X、Y、Z、W四种短周期元素在元素周期表的位置如图.其中W的原子序数是Y的2倍. A、B、C、D、E、F六种元素的原子序数依次增大.A的最高正价和最低负价的绝对值相等.B的基态原子有3个不同的能级且各能级中电子数相等.D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍.请回答下列问题:
A、B、C、D、E、F六种元素的原子序数依次增大.A的最高正价和最低负价的绝对值相等.B的基态原子有3个不同的能级且各能级中电子数相等.D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍.请回答下列问题: