��Ŀ����
X��Y��Z��W��ǰ20��Ԫ�أ�ԭ��������������X��ԭ�Ӱ뾶��С��Ԫ�أ�YԪ��ԭ�ӵ������������ǵ��Ӳ�����2����ZԪ�ص�-1�������ӵĺ�������Ų�����ԭ����ͬ��WԪ��Ϊ����������ij�ֻ����������������������˵��������ǣ�������
| A��X��Y�γɵĻ������п��ܺ���˫�� |
| B��X���ʺ�Z�����ڰ����ܾ��ҷ�Ӧ |
C��WԪ����ZԪ���γɵĻ������õ���ʽ��ʾ�γɹ���Ϊ��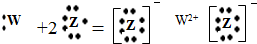 |
| D��XZ�ķе�����Zͬ�������X�Ļ���������� |
���㣺ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������X��Y��Z��W��ǰ20��Ԫ�أ�ԭ��������������X��ԭ�Ӱ뾶��С��Ԫ�أ���XΪHԪ�أ�YԪ��ԭ�ӵ������������ǵ��Ӳ�����2����Yԭ��ֻ����2�����Ӳ㣬����������Ϊ4����YΪCԪ�أ�ZԪ�ص�-1�������Ӻ�������Ų�������ԭ����ͬ����ZΪF��WԪ��Ϊ����������ij�ֻ��������������������WΪCa���ݴ˽��
���
�⣺X��Y��Z��W��ǰ20��Ԫ�أ�ԭ��������������X��ԭ�Ӱ뾶��С��Ԫ�أ���XΪHԪ�أ�YԪ��ԭ�ӵ������������ǵ��Ӳ�����2����Yԭ��ֻ����2�����Ӳ㣬����������Ϊ4����YΪCԪ�أ�ZԪ�ص�-1�������Ӻ�������Ų�������ԭ����ͬ����ZΪF��WԪ��Ϊ����������ij�ֻ��������������������WΪCa��
A��X��Y�����γɻ�����C2H4��������̼ԭ��֮���γ�˫������A��ȷ��
B������������ڰ����ܾ��ҷ�Ӧ����B��ȷ��
C��WԪ����ZԪ���γɵĻ�����ΪCaF2���õ���ʽ��ʾ�γɹ���Ϊ�� ��ѡ����Ca�ĵ���ʽ��д����C����
��ѡ����Ca�ĵ���ʽ��д����C����
D��HF����֮�����������е���ͬ�������Ԫ���⻯���D��ȷ��
��ѡC��
A��X��Y�����γɻ�����C2H4��������̼ԭ��֮���γ�˫������A��ȷ��
B������������ڰ����ܾ��ҷ�Ӧ����B��ȷ��
C��WԪ����ZԪ���γɵĻ�����ΪCaF2���õ���ʽ��ʾ�γɹ���Ϊ��
 ��ѡ����Ca�ĵ���ʽ��д����C����
��ѡ����Ca�ĵ���ʽ��д����C����D��HF����֮�����������е���ͬ�������Ԫ���⻯���D��ȷ��
��ѡC��
���������⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ���ע���õ���ʽ��ʾ��ѧ�������ʵ��γɣ�ע��������������ʵ�Ӱ�죬�Ѷ��еȣ�

��ϰ��ϵ�д�
 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д�
�����Ŀ
��NO2װ����������ܱ������У�����Ӧ2NO2��g��?N2O4��g���ﵽƽ��ı�����һ������������������ȷ���ǣ�������
| A�������¶ȣ�������ɫ�����˷�ӦΪ���ȷ�Ӧ |
| B������ѹ�����������ƽ�������ƶ������������ɫ��dz |
| C������ѹ������������������Сһ�룬ѹǿ����С��ԭ�������� |
| D�����º���ʱ�����������������壬ѹǿ����ƽ�������ƶ�������������ɫ��dz |
��NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ�������
| A����״���£�22.4L��H2O�к��еķ�����ΪNA |
| B�����³�ѹ�£�48g O3��O2��������к���ԭ����Ϊ3NA |
| C��12g Mg������ϡ���ᷴӦת�Ƶĵ�����Ϊ2NA |
| D��1L 1mol?L-1Na2CO3��Һ�к��е���������ΪNA |
ͭ��һ������Ҳ�����⣬����Ҫ�ɷ���ͭ�̣���ѧʽΪCu2��OH��nCO3��ʽ��n���ڣ�������
| A��1 | B��2 | C��3 | D��4 |
��NA��ʾ�����ӵ�������ֵ��������������ȷ���ǣ�������
| A��78g������̼̼˫������ĿΪ3NA |
| B�����³�ѹ�£�22.4L������̼���е�ԭ������Ϊ3NA |
| C��1mol Fe������ϡHNO3��Ӧ��ת��3NA������ |
| D��1L 1mol?L-1��NaClO��Һ�к���ClO-����ĿΪNA |
����������25��ʱ��ˮ��Һ�еĵ���ƽ�ⳣ��������ѡ����ȷ���ǣ�������
| ���� | �����ᣨHCN�� | ̼�ᣨH2CO3�� | ����ᣨHF�� |
| ����ƽ�ⳣ��Kֵ | 6.2��10-10��K�� | 4.2��10-7��K1�� 5.6��10-11��K2�� |
6.61��10-4��K�� |
| A����������Һ��ͨ�����CO2 F-+H2O+CO2=HF+HCO3- |
| B��Na2CO3��Һ��2C��Na+��=C��CO32-��+C��HCO3-��+C��H2CO3�� |
| C���к͵��������pH�������ᣨHCN��������ᣨHF������NaOH����ǰ�ߴ��ں��� |
| D����Ũ�ȵ�NaCN��NaF��Һ��PHֵǰ��С�ں��� |
