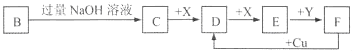题目内容
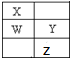 W、X、Y、Z为短周期元素,在周期表中的位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )
W、X、Y、Z为短周期元素,在周期表中的位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )| A、常压下四种元素的单质中,X的非金属性最强 |
| B、四种元素都能与氧元素形成稳定的化合物 |
| C、Y、Z 离子最外层电子数相同 |
| D、Y元素具有两性元素 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:W、X、Y、Z为短周期元素,由元素在周期表中的位置可知,X为H元素、W为Li、Y为Be、Z为Mg,结合元素化合物性质解答.
解答:
解:W、X、Y、Z为短周期元素,由元素在周期表中的位置可知,X为H元素、W为Li、Y为Be、Z为Mg,
A.四元素中,只有H为非金属元素,Li、Be、Mg为金属元素,故H元素非金属性最强,故A正确;
B.H、Li、Be、Mg都能与氧元素形成稳定的化合物,故B正确;
C.Be2+离子最外层电子数为2,Mg2+离子最外层电子数为8,两离子最外层电子数不相同,故C错误;
D.根据对角线原则,Be与Al的性质相似,是两性元素,故D正确,
故选C.
A.四元素中,只有H为非金属元素,Li、Be、Mg为金属元素,故H元素非金属性最强,故A正确;
B.H、Li、Be、Mg都能与氧元素形成稳定的化合物,故B正确;
C.Be2+离子最外层电子数为2,Mg2+离子最外层电子数为8,两离子最外层电子数不相同,故C错误;
D.根据对角线原则,Be与Al的性质相似,是两性元素,故D正确,
故选C.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,需要学生熟练掌握元素周期表的结构,难度不大.

练习册系列答案
相关题目
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
A、异戊二烯(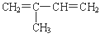 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |
| B、CH3CH2CH2Cl在碱性溶液中水解 |
| C、甲苯在一定条件下发生硝化生成一硝基甲苯的反应 |
| D、2-氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应 |
下列说法中不正确的是( )
| A、煤、石油、天然气均为化石能源 |
| B、化石能源是可再生能源 |
| C、直接燃烧煤不如将煤进行深加工后再燃烧效果好 |
| D、化石燃料在燃烧过程中能产生污染环境的SO2等有害气体 |
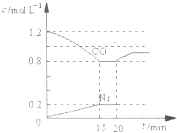
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )


| A、原子半径:Z>Y>X |
| B、R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
| C、X和Z形成的化合物能溶于NaOH溶液 |
| D、Y和W形成的化合物中,阴阳离子的个数可能比为1:1 |
已知H2A为弱酸,下列说法错误的是( )
| A、0.1mol/L的Na2A溶液中:c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
| B、常温下,将pH=3的H2A溶液稀释到原来的100倍,则稀释后溶液的pH<5 |
| C、常温下,将pH=3的H2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性 |
| D、常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na+)-c(HA-)-c(A2-)=10-5-10-9 |

 已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质:Y在常温下为液态,E的相同对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去);
已知B是一种由三种短周期(各位于不同周期)元素组成的正盐,该盐在常用锌锰干电池中做电解质:Y在常温下为液态,E的相同对分子质量比D大16,它们存在如下转化关系(反应条件及部分产物已略去);