题目内容
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )


| A、原子半径:Z>Y>X |
| B、R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
| C、X和Z形成的化合物能溶于NaOH溶液 |
| D、Y和W形成的化合物中,阴阳离子的个数可能比为1:1 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R有+7、-1价,则R为Cl,据此解答.
解答:
解:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R有+7、-1价,则R为Cl,
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Na>Al>O,故A错误;
B.次氯酸的酸性比硫酸弱,故B错误;
C.氧化铝是两性氧化物,与氢氧化钠反应生成偏铝酸钠与水,故C正确;
D.Y和W形成的化合物Na2S、Na2S2中阴阳离子的个数比为1:2,故D错误,
故选C.
A.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Na>Al>O,故A错误;
B.次氯酸的酸性比硫酸弱,故B错误;
C.氧化铝是两性氧化物,与氢氧化钠反应生成偏铝酸钠与水,故C正确;
D.Y和W形成的化合物Na2S、Na2S2中阴阳离子的个数比为1:2,故D错误,
故选C.
点评:本题考查结构性质与位置关系、元素周期律等,难度不大,根据推断元素是解题的关键,根据化合价结合原子序数进行推断.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、1mol Cl2通入含有2mol FeI2的溶液中:2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 |
| B、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| C、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
| D、向银氨溶液中加入足量的盐酸:[Ag(NH3)2]++OH-+3H+═Ag++2NH4++H2O |
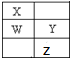 W、X、Y、Z为短周期元素,在周期表中的位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )
W、X、Y、Z为短周期元素,在周期表中的位置如图所示,有关元素W、X、Y、Z的叙述,不正确的是( )| A、常压下四种元素的单质中,X的非金属性最强 |
| B、四种元素都能与氧元素形成稳定的化合物 |
| C、Y、Z 离子最外层电子数相同 |
| D、Y元素具有两性元素 |
下列有关同分异构体数目的叙述不正确的是( )
| A、若甲苯苯环上的一个氢原子被一个含3个碳原子的烷基取代,所得产物有6种 |
B、与 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 |
| C、含有5个碳原子的饱和链烃,其一氯取代物共有8种 |
D、菲的结构简式为 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
为把溴水中溴单质萃取出来,应加入( )
| A、苯 | B、苯酚溶液 | C、乙醇 | D、乙醛 |
下列关于2mol?L-1 NaOH 溶液的说法中,不正确的是( )
| A、将80 g NaOH 溶于1 L水中,所得溶液中NaOH的物质的量浓度为2 mol?L-1 |
| B、1 L溶液中含2 mol NaOH |
| C、溶液中含2 mol钠离子和2 mol氢氧根离子 |
| D、溶液中钠离子的浓度是2 mol?L-1 |